Полімеризація — це назва хімічного процесу, який призводить до утворення макромолекул (великих молекул), які називаються полімерами, шляхом поєднання менших молекул — мономерів.
реакція полімеризація він дуже поширений у природі, як ми бачимо у вуглеводах (наприклад, крохмалі) і білках (як казеїн в молоці). Це також відбувається синтетично, оскільки переважна більшість полімерів, які люди використовують у повсякденному житті, виготовлені штучно.
Перший полімер, отриманий з полімеризація синтетичним був бакеліт у 1909 році бельгійським хіміком Лео Хендріком Бекеландом.
Загалом, щоб мономер з’єднався з іншим (незалежно від того, однакові вони чи різні) у реакції полімеризація, необхідно наявність вільної валентності (хімічний зв'язок, який необхідно виконати) в обох мономерах.
Ці валентності виникають в результаті розриву зв'язків за рахунок використання каталізаторів (наприклад, нікелю), зовнішніми умовами, такими як світло і тепло, або явищем резонансу в структурі (зсув електронів).
При формуванні поліпропілену (ПП полімеру), наприклад, використовується в домашньому посуді та іграшках,
пі посилання (π) у кожній молекулі розбивається наступним чином: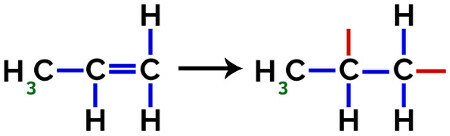
Розрив пі-зв'язку в пропілені
Таким чином, кожен пропіленовий мономер може зв’язуватися з двома іншими мономерами пропілену і утворювати полімер РР або поліпропілен (префікс полі вказує на кілька мономерних ланок). Найчастішим способом представлення полімеру є мономер між дужками і, зовні, буква n, яка вказує на кілька мономерів, як ми бачимо у випадку полімеру PP:
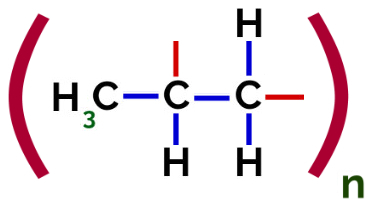
Представлення полімеру PP
реакція полімеризація можна зробити різними способами, як ми побачимо нижче:
а) Реакція аддитивна полімеризація
У цьому полімеризація, в мономері завжди відбувається розрив пі-зв’язку, що призводить до появи двох вільних валентностей в структурі, як при утворенні поліетиленові, полімер, широко використовується в фармацевтичній упаковці.
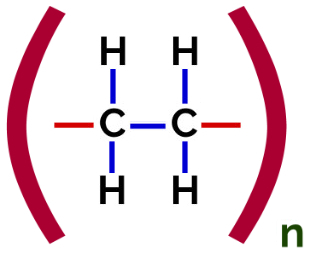
Структурна формула поліетилену аддитивного полімеру
В полімеризація поліетилену в якості мономеру використовуються молекули етилену (етилену), які мають пі-зв’язок між двома атомами вуглецю. Коли цей зв’язок розривається, з’являються дві вільні валентності, по одній на кожному атомі вуглецю, який був залучений до пі-зв’язку. Мономери об’єднуються саме в кожній із цих валентностей, тобто валентність одного пов’язана з валентністю іншого тощо.
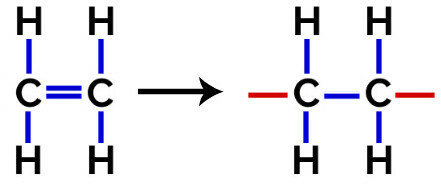
Рівняння утворення поліетилену
б) Реакція полімеризації приєднання 1.4
У цій полімеризації мономери мають дві подвійні зв’язки, що чергуються (один пі і один сигма), що сприяє цьому резонансу (змінювання положення пі-електронів пі-зв'язку), як при утворенні синтетичного каучуку (полібутадієну)

Структурна формула полібутадієну
Мономерною одиницею цього полімеру є бутадієн, який має дві подвійні зв’язки, що чергуються. При резонансі структура має подвійний зв’язок між вуглецю 2 і 3 і дві вільні валентності на вуглецю 1 і 4. Саме в цих вільних валентностях вуглецю 1 і 4 поєднуються мономери.

Бутадієновий резонанс
в) Реакція конденсаційна полімеризація або усунення
Це реакція полімеризація в якому, обов'язково, два мономери (однакові або різні) одночасно втрачають атоми або групи, в результаті чого в кожній з них утворюються дві вільні валентності. Таким чином, завжди відбувається видалення водню з мономеру, який потім з’єднується з галогеном (F, Cl, Br, I), OH, NH2, або до CN іншого мономеру.
Отже, в полімеризація при елімінації завжди відбувається утворення води, галогенованої кислоти (HCl, HI, HF, HBr), аміаку (NH3) або синильну кислоту (HCN) на додаток до полімеру. Дивіться, наприклад, уявлення про утворення поліестеру, матеріалу, який використовується як тканина:

Рівняння утворення поліестеру
Мономерами, що утворюють поліефір, є п-бензолдіова кислота та етан-1,2-діол. Ми можемо спостерігати це в цьому полімеризація відбувається видалення молекул води, оскільки два мономери мають два гідроксили. У цьому процесі кислота втрачає два гідроксили, а діаспирт втрачає лише водень зі своїх гідроксилів:

Структура поліестеру
Поліефірні мономери з’єднуються за допомогою кисню в спирті та вуглецю в карбоновій кислоті.
Від мене Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm