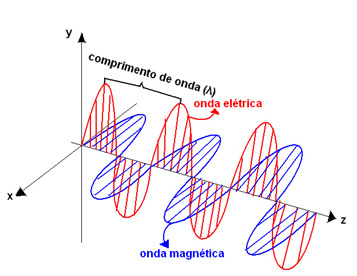
Серед міжмолекулярних сил індуковані дипольно-індуковані дипольні сили вони єдині, яких не досліджував нідерландський фізик Йоганнес Дідерік Ван дер Ваальс (1837-1923). Їх з’ясував німецький фізик Фріц Вольфганг Лондон (1900-1954), тому ці сили ще називають лондонські сили або лондонські сили дисперсії. Інша назва цих сил миттєвий диполь-індукований диполь.
Така сила виникає в неполярні речовини, наприклад, H2, O2, F2, Cl2, CO2, CH4 і C2H6, серед інших. І вони також можуть виникати між атоми благородного газу, коли вони наближаються, викликаючи відштовхування між їх електросферами. Таким чином електрони накопичуються на певній стороні, яка негативно поляризується, а протилежна – позитивно, через дефіцит негативного заряду.
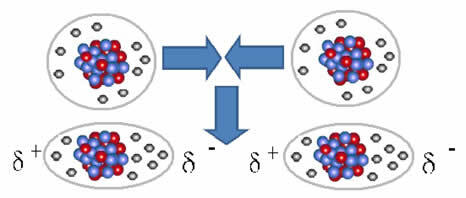
Неполярні молекули можуть переходити з газоподібного стану – в якому вони дуже далеко один від одного і немає взаємодії, оскільки немає полюсів – у рідкий і твердий стан. У цих агрегатних станах молекули знаходяться ближче, і електронне тяжіння або відштовхування між їх електронами і ядра можуть призвести до деформації їх електронних хмар, миттєво породжуючи позитивні та негативні полюси тимчасовий.
Миттєві диполі можуть викликати поляризацію сусідніх молекул, у результаті чого виникають сили притягання.
Не зупиняйся зараз... Після реклами ще більше ;)
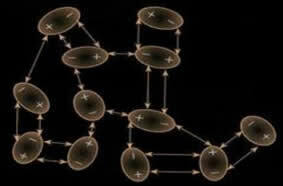
Ця індукція також може виникнути. між різними молекулами і взагалі ці сили слабші за інтенсивністю ніж міцність диполь-дипольного та водневого зв’язку. Тому тверді речовини з такою силою взаємодії, такі як сухий лід (вуглекислий газ - CO2) і йод (I2), які перебувають у твердому стані, підвищуються (переходять у газоподібний стан); оскільки енергія, необхідна для порушення їхньої взаємодії, мала.
Приклад міжмолекулярних сил між полярними і неполярними молекулами є між газоподібним киснем (неполярний) і водою (полярний). Виявляється, що негативний кінець води наближається до О2, відштовхуючи себе, і, таким чином, електронна хмара неполярної молекули віддаляється. Потім кисень на мить поляризується і починає взаємодіяти з водою, розчиняючись у ній.
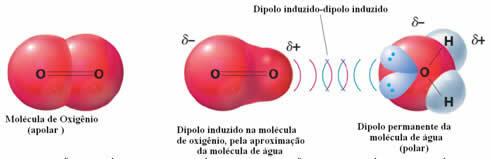
Оскільки ці сили слабкі, розчинність цього газу у воді мала. Незважаючи на це, його присутність необхідна для збереження життя різних водних організмів.
Ця сила взаємодії також зустрічається в природі, забезпечуючи зчеплення між лапами геконів і поверхнею, по якій вони ходять. Тому вони можуть ходити по стінах і стелі, не впавши і не прилипаючи.
Автор: Дженніфер Фогаса
Закінчив хімію
Шкільна команда Бразилії
Чи хотіли б ви посилатися на цей текст у шкільній чи академічній роботі? Подивіться:
ФОГАЧА, Дженніфер Роша Варгас. «Індукований диполь-індукований диполь або лондонські дисперсійні сили»; Бразильська школа. Доступний у: https://brasilescola.uol.com.br/quimica/forcas-dipolo-induzido-dipolo-induzido-ou-dispersao-london.htm. Доступ 27 липня 2021 року.