THE розчинністьможна визначити як максимально можлива кількість розчиненої речовини, яку можна розчинити в певній кількості розчинника при даній температурі.
Ця максимальна кількість, яку можна розчинити, також відома як коефіцієнт розчинності або ступінь розчинності. Але розчинність будь-якої речовини залежить, крім іншого, від типу розчинника, в якому розчинена речовина диспергована.
Наприклад, NaCl (хлорид натрію - кухонна сіль) дуже добре розчиняється у воді, і в 1 л води при 20ºC ми можемо розчинити до 360 грамів цієї солі. Але коли розчинник перетворюється на бензин, при однакових умовах об’єму, температури і тиску сіль не розчиняється.
Чому розчинність речовини так сильно відрізняється від одного розчинника до іншого?
Одним із факторів є полярність залучених сполук. У наведеному прикладі маємо, що сіль полярна, вода полярна, а бензин неполярний. Сіль утворена атомами натрію (Na) і хлору (Cl), які зв’язуються іонними зв’язками, в яких натрій безумовно віддає електрон хлору, утворюючи іони Na.
+ і Cl-. Оскільки ці іони мають протилежні заряди, вони притягуються та утримуються разом (Na+кл-).
Це показує нам, що сіль насправді полярна, кожен іонний зв’язок полярний, оскільки в з’єднанні існує різниця в електричному заряді.
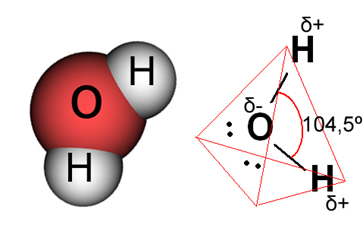
У випадку з водою існуючий зв’язок є ковалентним, у якому два атоми водню мають спільні електрони з атомом кисню. Молекула води має два диполі, причому кисень має частково негативний заряд, а водень — частково позитивний (δ- O ─ H δ+). Але ці диполі не компенсують один одного, тому що молекула води зустрічається під кутом 104,5º, що показує, що розподіл і заряд уздовж молекули нерівномірні. На атомі кисню в молекулі є більша негативна щільність заряду. Це показує нам, що молекула води дійсно полярна.
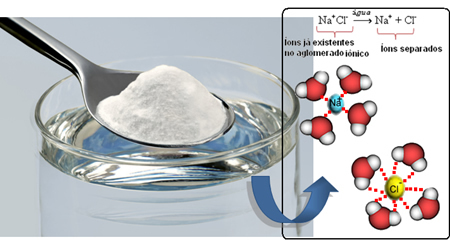
Отже, коли ми змішуємо сіль з водою, позитивна частина солі, яка є катіонами Na.+, притягується негативною частиною води, якою є кисень, і негативною частиною солі (аніони Cl-) притягується позитивною частиною води (H+). Отже, союз Na+кл- він розщеплюється, розчиняючи сіль у воді.
Бензин, навпаки, утворений сумішшю різних вуглеводнів, які є неполярними, тобто розподіл електричного заряду бензину рівномірний. Таким чином, не відбувається взаємодії іонів солі з бензином і він не розчиняється.
Ці та інші подібні випадки приводять нас до наступного висновку:

Однак це не можна вважати загальним правилом, оскільки є багато випадків неполярних розчинених речовин, які добре розчиняються в полярних розчинниках і навпаки. Отже, щоб зрозуміти, чому це відбувається, ми повинні розглянути ще один фактор: тип міжмолекулярна сила розчинника і розчиненої речовини.
Закон про це в тексті: «Зв'язок між молекулярною міцністю та розчинністю речовин”.
Автор: Дженніфер Фогаса
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/relacao-entre-polaridade-solubilidade-das-substancias.htm

