Kps - це скорочення, що використовується для позначення постійна продукту розчинності, що відноситься до добутку (множення) концентрації в кількості речовини іонів, присутніх у розчині.
Щоразу, коли до розчинника, такого як сульфат барію, додається погано розчинна розчинена речовина, невелика кількість частина цієї солі розчиняється у воді, а решта накопичується на дні ємності, утворюючи тіло фон. Страждає сіль, яка розчиняється дисоціація, виділяючи у воду катіони та аніони.

Осад, присутній у розчині з водою та сульфатом барію
До того ж сіль не представляє користі розчинність, кількість розчиненої розчиненої речовини з часом не змінюється, оскільки між іонами солі (присутніми в розчині) та фоновим тілом існує рівновага розчинення.

Баланс розчинення BaSO4 у воді
Kps розчиненої речовини
О Kps розчиненої речовини є добутком молярних концентрацій іонів-учасників. Завжди необхідно підвищувати концентрацію іонів до відповідного стехіометричного коефіцієнта (використовується для збалансування рівняння).
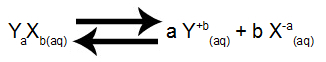
Рівновага розчинення електроліту YXB
О Kps пропонованої рівноваги для солі YXB у ньому буде концентрація реагенту Y (підвищена до його стехіометричного коефіцієнта (a) та концентрація продукту X (підвищена до його стехіометричного коефіцієнта (b)).
Kps = [Y+ b]. [X-The]B
Приклад
Припустимо, ми готуємо розчин з водою та ціанідом алюмінію [Al (CN)3], яка є практично нерозчинною у воді сіллю. Коли цю сіль додають у воду, вона закінчується явищем дисоціації.

Рівновага розчинення електроліту Al (CN)3
Отже, через рівняння рівноваги розчинення солі ми маємо, що воно Kps матиме множення концентрації катіона алюмінію (Al+3), підвищений до показника 1 концентрацією ціанідного аніона (CN-1) піднято до показника 3.
Kps = [Al+3]1. [CN-1]3
Kps значення розчиненої речовини
Коли ми знайдемо Kps певної солі, змішаної з водою, ми також знаємо концентрацію кожного з іонів у розчині. За цими даними ми можемо визначити рейтинг розчину або поведінку розчиненої речовини в розчині. Розглянемо наступний баланс:
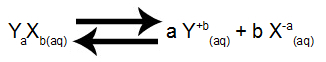
Рівновага розчинення електроліту YXB
Ми можемо встановити такі відносини:
Якщо Kps = [Y+ b]. [X-The]B = 0, маємо насичений розчин без присутності осаду;
Якщо Kps> [Y+ b]. [X-The]B = 0, ми маємо ненасичений розчин, тобто малу кількість розчиненої речовини, розчиненої в розчиннику (по відношенню до коефіцієнт розчинності);
Якщо Kps + b]. [X-The]B = 0, ми маємо насичений розчин з днищем, тобто відбудеться випадання осаду електроліту (розчиненої речовини);
Якщо значення Kps електроліту занадто низьке, це погано розчинний матеріал у розчиннику.
Приклад Розрахунок Kps розчиненої речовини
(UERN): Розчинність нітрату кальцію [Ca (NO3)2] у воді - 2,0. 10–3 моль / літр при певній температурі. Kps цієї солі при тій же температурі становить:
а) 8.10–8.
б) 8.10–10.
в) 3.2.10–10
г) 3.2.10–8
Дані вправи:
Формула солі: Ca (NO3)2;
Молярна концентрація солі (розчинність): 2,0. 10–3 моль / л.
Щоб вирішити і обчислити Kps, вам потрібно зробити наступне:
Крок 1: Налаштуйте баланс розчинення солі.
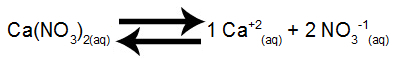
Рівновага розчинення нітрату кальцію у воді
Нітрат кальцію під час дисоціації у воді виділяє 1 моль катіонів кальцію (Ca+2) і 2 моль нітратних аніонів (NO3-1).
Крок 2: Складіть вираз Kps солі
Kps цієї солі буде добутком концентрації катіону кальцію, підвищеної до показника 1 на концентрацію нітратного аніона, піднятого до показника 2, як показано нижче:
Kps = [Ca+2]1.[БІЛЯ3-1]2
Крок 3: Визначте значення концентрацій іонів у розчині
Для розрахунку Kps нам потрібні значення концентрацій іонів, проте вправа забезпечила молярність солі в розчині. Щоб визначити концентрацію кожного іона, просто помножте молярність солі на стехіометричний коефіцієнт учасника реакції:
Для катіону кальцію:
[Ось+2] = 1. 2,0. 10–3
[Ось+2] = 2,0. 10–3 моль / л
Для нітратного аніона:
[БІЛЯ3-1] = 2. 2,0. 10–3
[БІЛЯ3-1] = 4,0. 10–3 моль / л
Крок 4: Використовуйте значення концентрації, знайдені на кроці 3 у виразі Kps (визначені на кроці 2).
Kps = [Ca+2]1.[БІЛЯ3-1]2
Kps = [2.10-3]1.[4.10-3]2
Kps = 2,10-3.16.10-6
Kps = 32,10-9
або
Kps = 3.2.10-9 (міс / л)
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kps.htm

