Деякі сполуки мають у своїй структурі подвійні зв'язки, що чергуються з одинарними. Найвідоміший з них - бензол, структура якого була запропонована в 1865 р. Німецьким хіміком Фрідріхом Августом Кекуле (1829-1896). Його структура буде циклічною і утворена трьома подвійними зв’язками впереміш з трьома одинарними зв’язками, як показано на малюнках нижче:
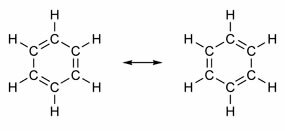
Обидва способи представлення бензолу є прийнятними, оскільки можна змінювати електрони в π-зв’язках, не змінюючи положення атомів. Однак ні представляє, що саме він є, ні пояснює його поведінку. Він повинен поводитися як алкен і викликати реакції додавання, але на практиці цього не відбувається. Бензол досить стабільний і діє так, ніби не має подвійних зв'язків; він дає реакції заміщення, як у алканах.
У 1930 році американський вчений Лінус Полінг запропонував теорію резонансу, яка пояснювала це очевидне протиріччя. Ця теорія сказала:
«Кожного разу, коли в структурній формулі ми можемо змінити положення електронів без зміни положення атомів, реальна структура немає не буде жодною з отриманих структур, скоріше a резонансний гібрид цих структур ".
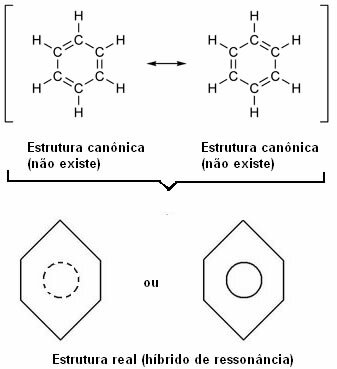
Про цей ефект свідчать розмір вуглецевих зв’язків та відстань між ними. Ця відстань є проміжною до віддалі одинарного зв’язку (1,54 Å) та подвійного зв’язку (1,34 Å); будучи, отже, 1,39 Å, завдяки ефекту резонансу.
Цей ефект також можна побачити в структурі молекули озону (O3), як показано нижче:
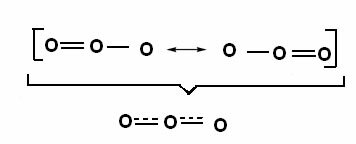
Канонічні структури та озонорезонансні гібриди.
Дженніфер Фогача
Закінчив хімію
Шкільна команда Бразилії.
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/ressonancia-compostosquimicos.htm

