Періодична система - це спосіб впорядкувати всі хімічні елементи за їх властивостями та показати деяку інформацію про них.
У повсякденному житті організація дуже важлива, щоб полегшити наше життя. Наприклад, уявіть свою шафу безладною, з шкарпетками, змішаними з сорочками та штанами. Це було б дуже важко, і знадобилося б більше часу, щоб знайти конкретний носок, який ви хотіли одягнути, правда? Але якщо ви організуєте свій гардероб і покладете всі шкарпетки в одну шухляду, знайдіть шухляду. для футболок, іншого для шортів тощо, знайти набагато простіше буде потрібно. І чим більше у вас одягу, тим більше потрібно організації.
Так само вчені з часом відкрили багато хімічних елементів. Щоб дати вам уявлення, у 1850 році було відомо близько 60 елементів, але сьогодні ми знаємо про існування 118. Таким чином, виникла потреба організувати ці хімічні елементи таким чином, щоб полегшити розуміння їх властивостей. У цьому полягає роль Періодичної системи хімічних елементів.
Періодична система, яку ми використовуємо сьогодні, розташована горизонтальними лініями у порядку зростання атомного номера.
Вам слід звертатися до Періодичної таблиці так, ніби ви читаєте звичайний текст, тобто завжди починається з першого ряду і з лівого боку направо, а потім продовжується вниз до наступного ліній.Хімічні елементи були розміщені на Періодичній системі окремими квадратами, де символ елемента знаходиться в половина, а значення атомного номера зазвичай пишеться вгорі, як показано в прикладі водню нижче:

Символ водню та його атомний номер, як показано в Періодичній системі
Атомний номер - це кількість протонів або позитивних зарядів, які мають атоми елемента. Це значення дорівнює кількості електронів, коли атом знаходиться в основному стані.Водень - це елемент, який має лише 1 протон, тобто його атомний номер дорівнює 1. Отже, водень - це перший елемент, розміщений у таблиці. Наступним елементом, що знаходиться на тій самій лінії, що і водень, є гелій, оскільки він має атомне число, рівне 2.
Переходячи до нижнього ряду, першим є літій з атомним числом, рівним 3, поруч - берилій з атомним номером 4 тощо.Подивіться на перші рядки Періодичної системи, показані нижче, і переконайтеся, що порядок атомного номера зростає в самий раз.
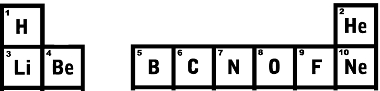
Перші два рядки Періодичної системи
У Періодичній системі є сім рядків, і вони називаються періоди. Подивіться:

Періодична система періодів
Є 18 стовпців, які називаються сім'ї або групи. Важливим аспектом є це елементи, що належать до одного сімейства - це ті, що мають подібні фізичні та хімічні властивості.

Сім'ї та групи періодичної системи
Давайте подивимось, чи зрозуміли ви? Скажіть, який хімічний елемент належить до 4-го періоду, а до сім’ї 16?
Якщо ви сказали Se (селен), ви маєте рацію! А тепер скажи мені, який його атомний номер. Правильно, це 34.
У кожному маленькому квадратику, який бачить елемент, є також інша важлива інформація, така як атомна маса та електрони які знаходяться в кожному електронному шарі атомів. Наприклад, див. На наступному зображенні, що неон має символ Ne, його атомний номер дорівнює 10, атомна маса дорівнює 20,1797 u і його електрони розподіляються так у своїх шарах: 2 - 8, тобто в шарі, найближчому до ядра, є два електрони, а в найдальшому - вісім електрони.

Неоновий символ на Періодичній системі та його атом
Тепер зверніть увагу на два цікаві аспекти: (1) неон лише має дві орбіти або шари, де знаходяться ваші електрони, ось чому він займає 2-й період (2-й рядок);і (2) він має вісім електронів на останньому шарі, тому він це сім'я 18.
Це показує нам наступне:
* Елементи, що знаходяться в одному періоді періодичної системи, мають однакову кількість електронних шарів і можуть мати максимум сім;
* Хімічні елементи, що знаходяться в одному сімействі періодичної системи, мають однакову кількість електронів в останній електронній оболонці:
* Сім'я 1: є все 1 електрон в останньому електронному шарі;
* Сім'я 2: є все 2 електрони в останньому електронному шарі;
* Сім'я 13: є все 3 електрони в останньому електронному шарі;
* Сім'я 14: є все 4 електрони в останньому електронному шарі;
* Сім'я 15: є все 5 електронів в останньому електронному шарі;
* Сім'я 16: є все 6 електронів в останньому електронному шарі;
* Сім'я 17: є все 7 електронів в останньому електронному шарі;
* Сім'я 18: є все 8 електронів в останньому електронному шарі.
Деякі групи чи сім’ї в Періодичній системі отримують конкретні імена, див. Деякі:
Сім'я 1: Лужні метали;
Сім'я 2: Лужноземельні метали;
Сім'я 16: Халькогени;
Сім'я 17: Галогени;
Сім'я 18: Благородні гази.

Організація сімей періодичної системи
Знову давайте перевіримо ваші знання. Дайте відповіді на наступні запитання, просто звернувшись до Періодичної системи:
1- Як називається родина хлору?
2- Який його атомний номер та атомна маса?
3- Скільки електронних шарів має атом хлору?
4- Скільки електронів має атом хлору в останній електронній оболонці?
Відповіді:
1- Галогени (сім'я 17).
2- Атомний номер хлору дорівнює 17, а його атомна маса дорівнює 35,45 u.
3- Атом хлору має три електронні шари, оскільки він належить до третього періоду таблиці.
4- Атом хлору має сім електронів у валентній оболонці, оскільки він належить до сімейства 17.
Існує ще одна важлива інформація, яку нам передає Періодична система, і про яку ми поговоримо в наступних текстах. Але розглянуті тут - головні, щоб ви почали розуміти, як в ній організовані елементи. Пам’ятайте, що стіл не призначений для прикраси, але ви повинні його добре знати, щоб мати змогу звернутися до нього у разі потреби.
Дженніфер Фогача
Закінчив хімію
Скористайтеся можливістю ознайомитись із нашими відео-класами, пов’язаними з предметом:


