Нітрати - це неорганічні сполуки, що містять аніон NO3-.
Азот із сімейства 15, має 5 електронів у валентній оболонці і повинен утворити три ковалентні зв’язки (із спільним використанням електронів) мати вісім електронів у валентній оболонці і таким чином залишатися стабільний. Однак кожен кисень має 6 електронів в останній оболонці, і тому кожен з його атомів повинен створити два зв’язки, щоб бути стабільним.
Отже, в нітратному аніоні азот є центральним елементом, який утворює подвійний зв’язок з одним із киснів, який є стабільним - одинарний зв’язок з одним із двох інших киснів, а з іншим - ковалентний зв’язок датив. Це означає, що один з кисню не є стабільним, і йому потрібно отримати ще 1 електрон, що дає загальний заряд, що дорівнює -1. З дативним азотом відбувається зв’язок більше, ніж він міг би зробити, віддаючи один із своїх електронів, отримуючи заряд, що дорівнює +1. Дивіться нижче структуру цього аніона:
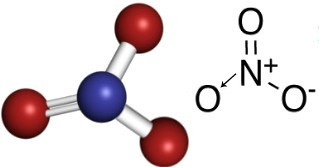
Цей аніон може отримувати електрон і утворювати електрично нейтральну сполуку - неорганічну сіль. Всі ці сполуки розчиняються у воді.
Основне застосування нітратів - у лікарських препаратах, таких як судинорозширювальні засоби для лікування стенокардії (болю в області спричинене низьким надходженням кисню через приплив крові до серцевого м’яза) та еректильною дисфункцією чоловічий. Вони також використовуються в добривах та вибухових речовинах, про що буде сказано далі.
Нітрати можуть утворюватися за допомогою реакції нейтралізації азотною кислотою (HNO).3) з деякою основою. Дивіться приклад нижче, де утворилася нітрат магнію:
HNO3 + Mg (OH)2 → Mg (НІ3)2+ H2О
Три основні приклади цього типу сполук: нітрат натрію (NaNO3), нітрат калію (KNO3) та аміачної селітри (NH4БІЛЯ3). У всіх цих випадках катіони (Na+, К+ і NH4+) забезпечують 1 електрон для нітратного аніона. Але насправді ці протилежні заряди притягують один одного і утворюють чітко визначені іонні скупчення, які є кристалічними гратами. Таким чином, нітрати зазвичай являють собою кристалічні тверді речовини, як показано нижче у випадку нітрату натрію:
Не зупиняйтесь зараз... Після реклами є ще щось;)
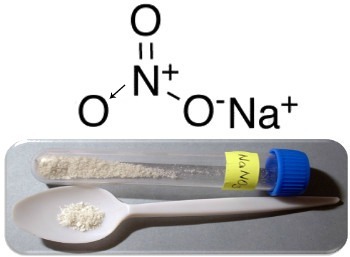
Ця сполука використовується у виробництві добрив, але в основному вона відома як Чилійська селітра, оскільки в чилійських пустелях є великі його родовища. Він перетворюється на нітрат калію, який використовується для виготовлення чорного порошку, що використовується в різних видах зброї та вибухових речовин.

І нітрат натрію, і нітрат калію називаються "селітрою", широко використовуючись як консерванти кольору консервів і копченостей, а також у деяких продуктах харчування для отримання більшої відчутності ситість. Однак їх споживання завдає серйозної шкоди здоров'ю, оскільки ці нітрати можуть перетворюватися бактеріями з організм на нітрити, а пізніше і на нітрозаміни, які є канцерогенними, в основному викликаючи рак у шлунку. Нітрити також перетворюють гемоглобіни в крові, роблячи їх нездатними переносити кисень.
Основними причинами надмірного споживання нітратів є використання азотних добрив при вирощуванні овочів.
Селітра також небезпечна тим, що збільшує концентрацію іонів натрію в організмі, що може спричинити такі проблеми із серцем, як високий кров'яний тиск.
О аміачна селітра він також використовується як добриво та вибухівка, і навіть використовувався з мазутом під час теракту на будівлі Світового торгового центру 11 вересня 2001 року.

У результаті нападу на Світовий торговий центр використана аміачна селітра *
* Авторські права на зображення: Ден Хауелл і Shutterstock.com
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Нітрати»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/nitratos.htm. Доступ 27 червня 2021 року.
Хімія

Повсякденні солі, карбонат кальцію, хлорид натрію, фторид натрію, нітрат калію, нітрат натрію натрій, карбонат натрію, бікарбонат натрію, бікарбонат натрію, сульфіт натрію, селітра, сода.