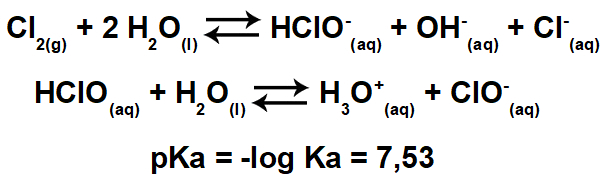Водні розчини солей можуть мати основний або кислотний характер, залежно від форми, в якій вони були отримані. Подивіться, через сольовий гідроліз, як кислотність і основність впливають на кінцевий продукт реакції:
Гідроліз солі сильної кислоти та слабкої основи
Реакція між сіллю та водою може утворювати сильну кислоту та слабку основу як продукти, див. Приклад:
Водний сольовий розчин нітрату амонію (NH4БІЛЯ3) має рН менше 7, дотримуйтесь його отримання:
NH4БІЛЯ3 (aq) + H2O (l) ↔ NH4OH (вод.) + HNO3 (тут)
Сильна кислота слабка основа
Гідроліз солі (NH4БІЛЯ3) утворює кислий розчин через наявність азотної кислоти (HNO3).
Сольовий гідроліз слабкої кислоти та слабкої основи
NH4CN (aq) + HOH (l) ↔ NH4OH (водний) + HCN (водний)
Слабка основа слабкої кислоти
Наведене вище рівняння представляє дисоціацію солі ціаніду амонію (NH4CN). Під час реакції утворюється слабка основа і кислота. І основа, і кислота не є іонізуючими, тобто вони не зазнають іонізації, отже, причина для класифікації.
Гідроліз солі сильною кислотою та сильною основою
NaCl (вод.) + HOH (л) ↔ NaOH (вод.) + HCl (вод.)
сильна сильна кислотна основа
Водний розчин солі NaCl (хлориду натрію) має нейтральний характер (pH = 7). Під час оборотної реакції, представленої вище, ми утворюємо гідроксид натрію (NaOH) та соляну кислоту (HCl), обидва класифіковані як сильні.
Не зупиняйтесь зараз... Після реклами є ще щось;)
Лірія Алвес
Закінчив хімію
Шкільна команда Бразилії
Побачити більше!
сольовий гідроліз - подивіться, як отримати слабку кислоту та сильну основу.
Рішення - Фізико-хімічна - Хімія - Бразильська школа
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
СУЗА, Лірія Алвес де. «Водний розчин солей»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/solucao-aquosa-sais.htm. Доступ 28 червня 2021 року.