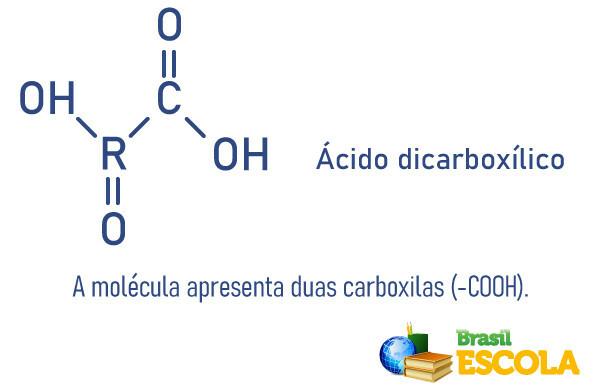
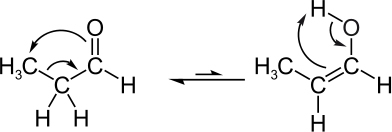
У 1874 р. Голландський хімік Якобус Енріке ва не Гофф (1852-1911) і французький хімік Жозеф Ахіле ле Бель (1847-1930) за допомогою математичних теорій самостійно припустили існування вуглецю асиметричний.
У той час їх жорстоко критикував, зокрема, не Гофф, відомий німецький хімік Адольф Вільгельм Кольбе (1818-1884). Однак Кольбе помилився, сьогодні ми знаємо, що існує асиметричний вуглець, настільки, що у 1901 році Вант Гофф був першим хіміком, який отримав Нобелівську премію.
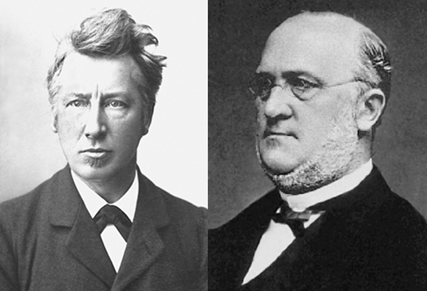
Ва не Гофф (ліворуч) і Кольбе (праворуч)
Однією з необхідних умов, щоб молекула мала оптичну активність, є її асиметричність. Крім того, одним із способів перевірити, чи є він асиметричним, є детальне вивчення його структури, щоб з’ясувати, чи є в ньому хоча б один асиметричний вуглець.
Що таке асиметрична молекула та асиметричний вуглець?
Щось симетричне - це те, що має принаймні одну площину симетрії. Наприклад, якщо ми розріжемо тенісну ракетку навпіл, дві отримані частини будуть абсолютно однаковими. Крім того, якщо ми розмістимо їх перед плоским дзеркалом, вони отримають ідентичне зображення.
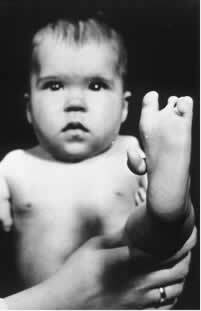
Називаються структури, які не підтримують площину симетрії асиметричний. Прикладом може служити наша рука, тому що якщо ми поставимо її перед дзеркалом, вона створить інший образ себе. Якщо ми покладемо праву руку, зображення буде лівою і навпаки. Іншим важливим моментом є те, що вони не перекриваються.
Не зупиняйтесь зараз... Після реклами є ще щось;)
Ось чому асиметричний вуглець ще називають хіральний вуглець, звідки походить це слово khéir що по-грецьки означає рука.
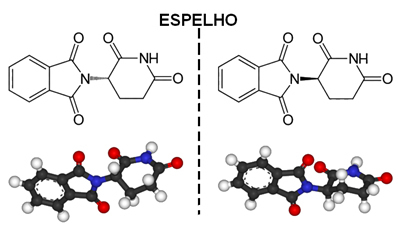
Прикладом асиметричної молекули є талідомід, структура якого наведена нижче:

Крапка, розташована зірочкою (*), відповідає асиметричному вуглецю він має чотири ковалентні зв’язки, які утворені з різними атомами або групами атомів.
Внизу знаходиться вуглець з чотирма різними лігандами перед дзеркалом. Зверніть увагу, що зображення не можна накладати на вихідну структуру:

Дві отримані вище молекули є оптичні ізомери або енантіомери.
Повертаючись до випадку талідоміду, внаслідок того, що він має асиметричний вуглець, результатом є те, що молекула починає мати не накладається зображення, яке відповідає іншій речовині. Отже, ми маємо два ізомери талідоміду з надзвичайно різними властивостями.
Один із цих (R) ізомерів має седативні властивості. Тому наприкінці 1950-х років його почали застосовувати як транквілізатор та засіб для сну для вагітних. Це спричинило трагедію, оскільки його (S) енантіомери також змішували з препаратом. Цей ізомер, у свою чергу, є тератогенним і призвів до того, що багато вагітних жінок мають своїх дітей з атрофованими руками, ногами, руками і ногами.
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Асиметричний або хіральний вуглець»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/carbono-assimetrico-ou-quiral.htm. Доступ 27 червня 2021 року.