Іноді це може статися мінімальна формула бути такою ж, як молекулярна формула сполуки; однак, це не завжди правда.
Наприклад, емпіричною або мінімальною формулою для води є Н2О, що вказує на те, що між елементами, що складають молекули води, існує співвідношення 2: 1. І, за збігом обставин, це також молекулярна формула води. Однак, щоб переконатися, що це трапляється не завжди, перегляньте наступні два приклади:
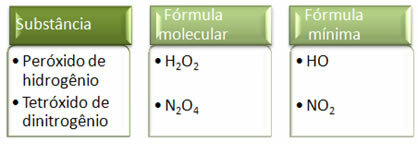
Оскільки мінімальна формула - це лише відношення атомів кожного елемента, а не фактична кількість їх у молекулярній формулі, це може відбуватися різних сполук, що мають однакову емпіричну формулу і навіть мінімальну формулу сполуки, може бути такою ж, як молекулярна формула інший. Зверніть увагу, у прикладі нижче, як це може статися:
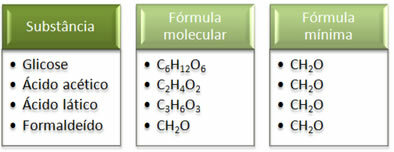
Дивіться, що мінімальна формула СН2Це однаково для всіх речовин, тобто ця мінімальна формула виражає, що, у всіх випадках, атоми вуглецю, водню та кисню присутні в молекулярних формулах у співвідношенні 1:2:1. Крім того, єдиним, хто має ту саму молекулярну формулу, що і емпірична формула, є формальдегід.
- Розрахунок мінімальної або емпіричної формули:
Щоб визначити емпіричну формулу сполуки, спочатку необхідно знати, який її відсоток або приблизна формула. Це можна зробити, вимірявши масу кожного елемента в 100 г зразка. Текст "Формула у відсотках або в центрі”З’ясовує це питання краще.
Не зупиняйтесь зараз... Після реклами є ще щось;)
Наприклад, припустимо, приблизний склад даної сполуки визначається як: 40,00% C, 6,67% H та 53,33% O. Ми передаємо ці значення у грами, враховуючи масу 100 г зразка компосту. Таким чином, ми маємо: 40 г С, 6,67 г Н і 53,33 г О.
Тепер необхідно передати ці значення на кількість речовини (моль). Ми робимо це шляхом ділення кожного знайденого значення на відповідну молярну масу:
С: 40/12 = 3,33
H: 6,67 / 1 = 6,67
O: 53,33 / 16 = 3,33
Оскільки значення не є цілими числами, ми використовуємо такий пристрій: ми ділимо всі значення на найменші з них, щоб пропорція між ними не змінювалася.
У цьому випадку найменше значення - 3,33, тож результат буде:
C: 3,33 / 3,33 = 1
В: 6,67 / 3,33 = 2
O: 3,33 / 3,33 = 1
Таким чином, мінімальна формула цієї невідомої речовини дорівнює: Ç1H2О1 або СН2О.
Коротко, кроки, необхідні для пошуку емпіричної або мінімальної формули речовини:

Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Мінімальна або емпірична формула"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Доступ 28 червня 2021 року.