Елементи або батареї, в яких основною складовою є літій, мають однією з характеристик той факт, що вони дуже легкі, оскільки літій є найменш щільним металом, виявленим на сьогодні. Щоб дати вам уявлення, цей сріблясто-білий метал плаває у воді, оскільки він вдвічі щільніший, ніж є. Це пов’язано з тим, що літій має лише три протони і три нейтрони.
Існує два основних типи літієвих акумуляторів, один з яких називається літієва йодна батарея. В основному він був розроблений для використання в Росії кардіостимулятори, оскільки він дуже легкий, безпечний (не виділяє газів, оскільки герметично закритий), він має хороший довговічність (приблизно від 8 до 10 років), забезпечує напругу 2,8 В і високу щільність заряду (0,8 Вт / см3).
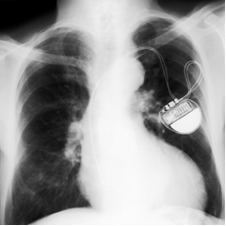
Електроди утворені літієм та йодним комплексом, які розділені кристалічним шаром йодиду літію, що дозволяє пропускати електричний струм. О металевий літій працює як анод цієї клітини, тобто негативний полюс окислюється, втрачаючи електрони. вже катод, позитивним полюсом, який зменшується, приймаючи електрони, є йодний комплекс.
Подивіться напівреакції, що відбуваються в електродах, і рівняння, яке представляє глобальну реакцію клітин цього типу:
Половина реакції анода: 2 Li(s) → 2 Я читав+(s) + 2e-
Напівреакція катода: 1 I2 (s) + 2e-→ 2 I-(s)
Глобальна реакція: 2 Лі(s) + 1 I2 (s) → 2 LiI(s)
Літій-йодні батареї мають форму дуже маленьких монет, як показано на малюнку нижче:

Інший тип комірок або акумуляторів - це іон літію. Цю назву вона бере саме тому, що в основі її роботи лежить рух іонів літію (Li+). В даний час він широко використовується в Росії акумулятори стільникових телефонів і його потенціал коливається від 3,0 до 3,5 В.
Не зупиняйтесь зараз... Після реклами є ще щось;)

Анод і катод утворені атомами, розташованими у таких площинах, як листи з просторами, куди вставляються іони літію. О анод утворюється графітом з металом міді, а іони інтеркалюються в площинах шестикутних вуглецевих структур, утворюючи наступну речовину: читатирÇ6. вже катод утворений іонами літію, інтеркальованими в оксиді з пластинчастою структурою (читатихCoO2).
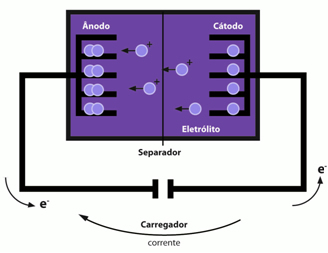
Таким чином, ми маємо, що іони літію залишають анод і мігрують через неводний розчинник до катода.
Половина реакції анода: LiрÇ6 (s) → y Li + Ç6+у-
Напівреакція катода: LiхCoO2 (s) + р читати+(s) + р і- → Я читавx + yCoO2 (s)
Глобальна реакція: ЛірÇ6 (s) + прочитатихCoO2 → Ç6(s) +читатиx + yCoO2 (s)
Ці акумулятори можна перезаряджати, просто використовуючи зовнішній електричний струм, який викликає міграцію іонів літію в протилежному напрямку, тобто від оксиду до графіту.

Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Літієві батареї та батареї»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/pilhas-baterias-litio.htm. Доступ 28 червня 2021 року.
Хімія

Небезпека від акумуляторів, забруднення важкими металами, побутовою технікою та електронікою, акумуляторними батареями, Хімічний склад нікель-кадмієвих батарей, правильна утилізація батарей стільникових телефонів, загальний обсяг акумулятори