ти Вуглеводні складаються утвореними вуглець (C) та водень (H). Гнучкість вуглецю, який є основним елементом цих сполук, сприяє існуванню величезного різноманіття структур Отже, деякі властивості, такі як температура плавлення та температура кипіння, можуть відрізнятися між одними вуглеводнями та іншими.
В основному це молекули аполярний, с міцністьs міжмолекулярні індукований дипольний тип і щільність менше від води. Ідентифікація цих сполук може бути здійснена за допомогою номенклатури, яка відповідає правилам, встановленим Міжнародним союзом чистої та прикладної хімії (Iupac).
Читайте також: Вуглець - один з найпоширеніших елементів у Всесвіті
Властивості вуглеводнів

Полярність: вуглеводні без присутності гетероатомів є аполярний.
Міжмолекулярні сили: зв’язки між молекулами вуглеводню мають такий тип індукований дипол.
температура плавлення і ікипіння: вони змінюються залежно від розміру, функції та структурної організації молекули.
фізичний стан: за нормальних умов температури та тиску вуглеводні з чотирма або менше атомами вуглецю перебувають у газоподібному стані. Ті, у яких від 5 до 17 вуглеводнів перебувають у рідкому стані, а вуглеводні, що містять понад 17 вуглеводнів, є твердими речовинами.
Щільність: менше, ніж щільність води, тобто менше 1,0 г / см³.
Реактивність: аліфатичні та ненасичені вуглеводні погано реагують; ненасичені сполуки частіше реагують з іншими молекулами, а циклічні вуглеводні з кількістю вуглеводнів до п’яти дуже реактивні.
Класифікація вуглеводнів
Вуглеводні можна класифікувати за структурною організацією ланцюга та закладами.Ненасиченість - наявність подвійної (-іх) або потрійної зв'язку між вуглецями, - поява з'єднання типу pi (π). вже гілки вони схожі на «гілки», прикріплені до більшої вуглеводневої структури. Циклічні ланцюги також можуть містити гілки та / або ненасичення - структурна організація вуглеводнів із замкнутим ланцюгом утворює багатокутники, такі як квадрат, трикутник, гексан та ін.
Щодо розташування атомів, вуглеводень може мати нормальний або розгалужений ланцюг.
→ С вуглеводеньнормальна, лінійна або пряма: той, що має рядок, що має лише два кінці.

→ С вуглеводеньненавидить розгалужений: той, що має ланцюжок, що має більше двох кінців. Для того, щоб знати, де і що є гілками, важливо правильно вибрати головний ланцюг. Основний ланцюг повинен містити всі ненасичені речовини та гетероатоми (якщо такі є), так само, як найбільша кількість послідовних вуглеців. Вуглеці, які не містяться в основному ланцюгу, є гілками.
Приклад:

Щодо свого "закриття", вуглеводень може мати замкнутий, відкритий або змішаний ланцюг.
→ Ланцюгові вуглеводніs закритий або циклічний: ті, що мають ланцюги, в яких атоми організовують себе, утворюючи цикл, багатокутник або ароматичне кільце (замкнутий вуглеводень із змінними ненасиченнями). Не майте вільних кінців, якщо немає гілки. Кожна вершина багатокутника являє собою вуглець та відповідні водневі зв’язуючі речовини.
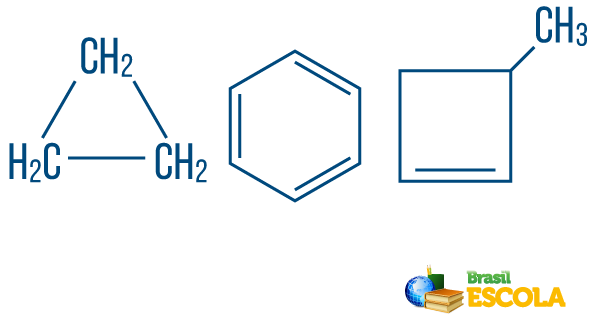
→ Відкритий ланцюг або ациклічні вуглеводні: це ті, що мають ланцюги, що мають принаймні два кінці.

→ Вуглеводень змішаний тип рядка: утворений кільцем або циклічним ланцюгом, прикріпленим до лінійної частини; він має принаймні один кінець.
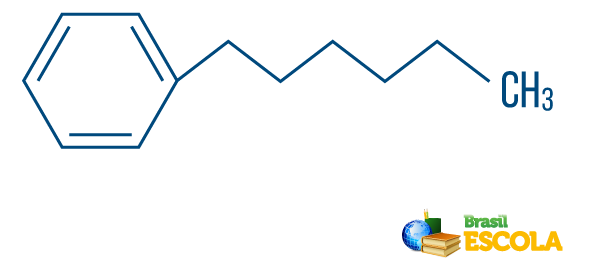
Читайте також: Ароматичні вуглеводні - приклади та властивості
Номенклатура вуглеводнів
Для кожного типу вуглеводнів існує правило іменування, встановлене Iupac. Номенклатура цих сполук складається наступним чином:
1-а частина: місцезнаходження та назва філій (ів) (за наявності);
2 частина: термін застосовується циклу якщо сполука є замкнутим ланцюгом, але якщо це аліфатичний (відкритий) ланцюг, це не буде необхідним;
3 частина: префікс, який вказує, скільки вуглецю є в основному ланцюгу;
4 частина: місце розташування та інфікс, що вказує на тип ненасиченості в молекулі;
5 частина: суфікс «o», властивий вуглеводням.
Якщо молекула має відкриту структуру, без розгалуження, номенклатура розпочнеться в частині 3.
У наступній таблиці наведена необхідна інформація (префікс, інфікс та суфікс) для вуглеводневої номенклатури загалом. О префікс змінюється залежно від кількості вуглецю; О інфікс, за кількістю ненасичень; це суфікс“О " відноситься до сполук вуглеводневого типу.
Префікс |
Інфікс |
Суфікс |
||
1 вуглець |
мет- |
Тільки одинарні дзвінки |
-an- |
-О |
2 вуглецю |
ет- |
|||
3 вуглецю |
підтримка |
1 подвійний зв’язок |
-en- |
|
4 вуглецю |
але- |
|||
5 вуглеців |
пент- |
2 подвійні зв’язки |
-дієн- |
|
6 вуглеців |
шістнадцятковий |
|||
7 вуглеців |
hept- |
1 потрійний зв’язок |
-в- |
|
8 вуглеців |
жовт- |
|||
9 вуглеців |
не- |
2 потрійних посилання |
-диїн- |
|
10 вуглеців |
грудня |
Першим кроком у розкритті номенклатури органічної сполуки є визначити основний ланцюжок вуглецю, який повинен містити ненасичені речовини і якомога більше послідовних вуглеводнів. Після ідентифікації основного ланцюжка, вуглець повинен бути перерахований - починаючи відлік з найближчої до гілок сторони та ненасичення (якщо такі є). THE локалізація буде числом вуглецю, де виявлено гілку або ненасиченість. Іноді існує лише одне можливе місце для радикального або подвійного або потрійного зв'язку, тому немає необхідності висловлювати розташування зв'язуючого вуглецю в номенклатурі.

THE номенклатура для філій буде задано кількістю вуглецю в кожному, плюс термінація лінія або ll. Коли існує більше однієї гілки, використовується алфавітний порядок.
Див. Приклади нижче:
→ Приклад 1
СН3 - СН2 - СН3 → Пропан
1-а частина: префікс “підтримка"Вказує, що ланцюг має три вуглеці.
2-а частина: інфікс "-an-”Сигналізує про те, що молекула встановлює лише зв’язки типу сигма або просто.
3-а частина: суфікс "-О”Характерно для вуглеводнів.
→ Приклад 2
СН2= СН-СН2-CH3 → Але-1-ен
У вуглеводнях з ненасиченістю необхідно нумерувати і знаходити вуглець, у якому знаходиться пара, і нумерація повинна бути якомога меншою. Для цього кількість вуглецю повинна починатися зі сторони, найближчої до подвійного зв'язку.
1-а частина: "але- " вказує на те, що в ланцюзі є чотири вуглеці.
2-а частина: "1-ru" відноситься до ненасиченості, розташованої між вуглецем 1 і 2.
3 частина: "-O" є характерним суфіксом вуглеводнів.
→ Приклад 3

1-а частина: "3-етил" сигналізує про наявність двовуглецевої гілки на вуглеці 2.
2-а частина: "-пент-" вказує на наявність п’яти вуглеводнів в основному ланцюзі.
3 частина: "-an-" - це інфікс, що застосовується до ненасичених ланцюгів (відсутні подвійні або потрійні зв’язки).
4 частина: "-O" є характерним суфіксом вуглеводнів.
→ Приклад 4
Для ланцюгів з більше однієї гілки, розмістіть радикали в номенклатурі в алфавітному порядку. Якщо в одній і тій самій молекулі є гілки та ненасичення, підрахунок вуглецю в основному ланцюзі слід проводити таким чином, щоб сума цифр розташування була якомога меншою.
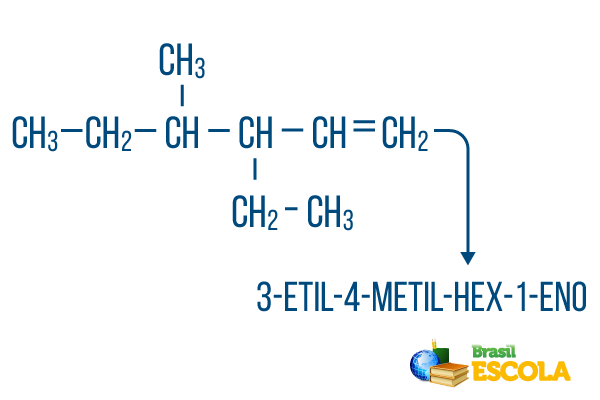
Підрахунок вуглецю в основному ланцюгу проводився зліва направо, а сума цифр ненасиченості та розташування гілок становить: 1 + 4 + 3 = 8. Якби кількість вуглецю була справа наліво, складена номенклатура була б такою 4-етил-3-метил-5-ен, чия сума локацій буде: 4 + 3 + 5 = 12, що перевищує іншу гіпотезу, тому її не слід використовувати.
1-а частина: 3-етил-4-метил робить посилання на радикали в алфавітному порядку та їх відповідне розташування.
2-а частина: шістнадцятковий означає, що в основному ланцюзі є 6 вуглеводнів.
3 частина: 1-ru вказує на наявність подвійного зв'язку на вуглеці 1.
4 частина: "-O" є характерним суфіксом вуглеводнів.
→ Приклад 5
Для закритих рядків правила іменування діють, але слово циклу починає назву сполуки, вказуючи, що це закритий або циклічний вуглеводень.
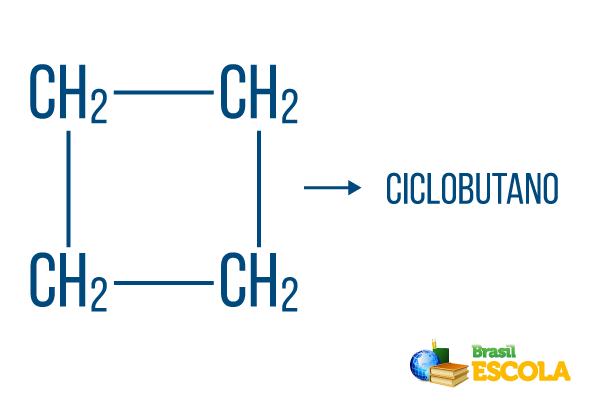
1-а частина: цикл- вказує, що це закритий рядок.
2-а частина: -но- позначає існування 4 ланцюгів вуглецю
3 частина: -Оє характерним суфіксом вуглеводнів.
Читайте також: Класифікація вуглецевих ланцюгів
Види вуглеводнів
Вуглеводні можна розділити на алкани, алкени, алкіни та алкадієни - які класифікуються як відповідно до встановлення ланцюга (подвійні (і) або потрійні зв’язки) - і циклани, які є ланцюгами зачинено.
→ Алкани: є вуглеводнями, які не мають ненасиченості. Загальна формула алканів - СнемаєH2n + 2, та немаєприкмета його складає префікс + an + О.
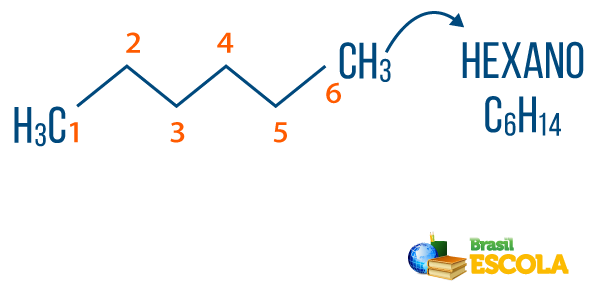
ти алкани можна зустріти в природі, як газ метан (СН4), який виділяється тваринами і виробляється в процесі розкладання, а також на нафтопереробних заводах та нафтохімічній промисловості. Сполуки типу пропан (Ç3H7), бутан (Ç4H10), з якого складається наш газ для приготування їжі (LPG), та октанові (Ç8H18), присутні в автомобільному паливі, є побічними продуктами Нафта.

→ алкени або алкени: це вуглецеві ланцюги, які мають ненасиченість, подвійний зв’язок. Загальна формула - CнемаєH2н, і ваш немаєприкмета його складає Pвиправити + en + o.

О етиленовий газ (Ç2H4), що використовується в сільському господарстві для прискорення дозрівання плодів, належить до функції алкен. З'єднання також використовується у виробництві сировини поліетилен, що використовується у виробництві пластмасового посуду.
→ Алкіни або ацетиленова: вуглеводні з потрійним зв’язком. Загальна формула - CнемаєH2n - 2. THE номенклатура його складає префікс + в + o.

О ацетилен або етин (C2H2) - газ алкінової функції, що використовується в зварні шви та розрізи металу. Ця сполука може досягати температури до 3000 ° C, що дозволяє проводити ремонт на занурених частинах корабля.

→ алкадієни або дієни: вуглецеві ланцюги з двома ненасиченнями, тобто двома подвійними зв’язками між вуглецями. Загальною формулою цієї функції є C.немаєH2n - 2. Зрозумійте, що це та сама формула, що і алкіни, а це означає, що це може статися ізомерія між сполуками (однакова молекулярна формула для різних сполук).
Номенклатура алкадієну складається з Pвиправити + дієн + о.
Приклад:

→ Вуглеводні із замкнутим ланцюгом: молекули організовуються циклічно, мають тенденцію утворювати багатокутник, і, як у відкритих ланцюгах, можуть існувати установи та / або наслідки. Циклони, цикли, цикліни та бензоли - вуглеводні із замкнутим ланцюгом.
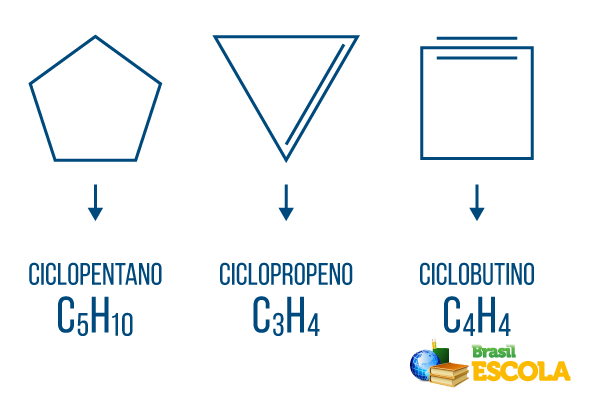
Циклони або циклоалкани: циклічні ланцюги, що складаються лише з одинарних зв’язків. Загальна формула - CнемаєH2н. Номенклатура: ciclo + префікс + an + o.
Цикли або циклоалкени: замкнуті вуглеводневі ланцюги з установою. Загальна формула - CнемаєH2n-2. Номенклатура: çiclo + префікс + en + О.
-
Цикліни або циклоалкіни: вуглеводні із замкнутим ланцюгом з наявністю двох подвійних зв’язків. Загальна формула - CнемаєH2n-4. Номенклатура: çiclo + префікс + в + o.
бензоли
Бензол являє собою тип вуглеводнів із замкнутим ланцюгом з шість вуглеців де облігації варіюються між одинарними та подвійними. Ці сполуки є токсичний і високо канцерогенні, використовуються як органічні розчинники в хімічних процесах.
Щоб вуглеводень вважався ароматичним, він повинен бути принаймні одним бензольне кільце, який є високореактивним, тому піддається двом або більше заміни, які ми побачимо тут як наслідки. Коли є два радикали, що зв’язують, ми будемо мати конкретні назви для кожної пари позицій.
Радіали на 1,2 вуглецю бензолу → орто
Радикали на 1,3 вуглецю бензолу → мета
Радіали на вуглеці 1,4 бензолу → для
Аноменклатура ароматичної сполуки проводиться наступним чином:
1-а частина: позиціонування лігандів (орто, мета або до).
2-а частина: назва радикала або радикалів, приєднаних до бензолу (метил, етил, пропіл…). Назва радикалів відповідає правилу інших вуглеводнів.
- 3 частина: -Bотрута, що є характерним терміном ароматичних вуглеводнів.
Приклади:
→ Орто-диметил-бензол

1-а частина: Оrto- вказує на те, що радикали розташовані на вуглецях 1 і 2.
2-а частина: -диметил- відноситься до двох радикалів, обидва з одним вуглецем.
3 частина: -бензол - характерний термін для ароматичних вуглеводнів.
→ Орто-етил-метил-бензол
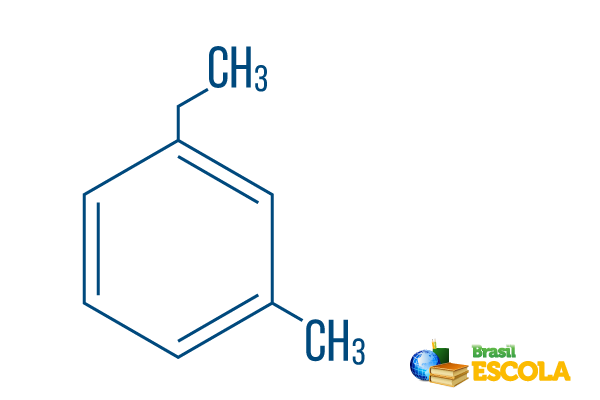
1-а частина: мох- вказує на те, що радикали розташовані на вуглецях 1 і 3.
2-а частина: етил-метил- відноситься до кількості вуглецю в кожному радикалі, тобто етил двовуглецева гілка і метил розгалуження одним вуглецем - розміщується в номенклатурі в алфавітному порядку.
3 частина: -бензол - характерний термін для ароматичних вуглеводнів.
→ Пара-діетил-бензол
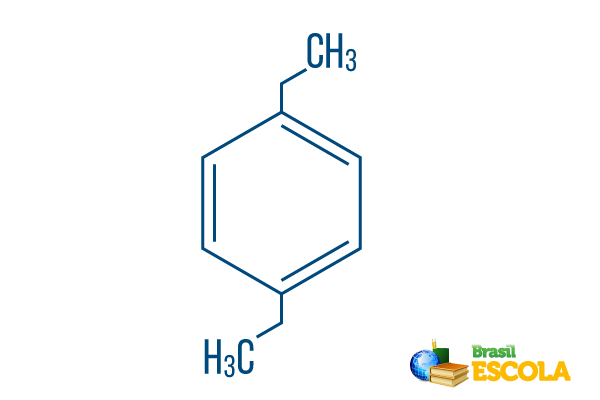
1-а частина: Pплуг- вказує, що радикали знаходяться на вуглецях 1 і 4 бензолу.
2-а частина: -діетил- посилається на два радикали цього типу етил, тобто дві гілки по два вуглецю кожна.
3 частина: -бензол - характерний термін для ароматичних вуглеводнів.
Читайте також:Відкриття структури бензолу
розв’язані вправи
(Unesp) - Октан - одна з основних складових частин бензину, який є сумішшю вуглеводнів. Молекулярна формула октану:
а) C8H18
б) C8H16
в) C8H14
г) C12H24
д) C18H38
Відповідь: буква а). Аналіз складеної номенклатури октан, це алкан, тобто молекула, що складається лише з одинарних зв’язків. Якщо загальною формулою алканів є СнемаєH2n + 2, замінивши "n" на вісім, що є кількістю вуглецю в основному ланцюзі - і унікальним у цьому випадку -, ми отримаємо, що молекулярна формула октану є C8H18.
(UFSCar-SP) - Розглянемо наступні твердження про вуглеводні.
I) Вуглеводні - це органічні сполуки, що складаються лише з вуглецю та водню.
II) Тільки ненасичені вуглеводні з прямим ланцюгом називаються алкенами.
III) Циклоалкани - це насичені аліфатичні вуглеводні із загальною формулою CnH2n.
IV) Є ароматичні вуглеводні: бромбензол, п-нітротолуол та нафталін.
Правильними є такі твердження:
а) Лише I та III.
б) Тільки I, III та IV.
в) лише ІІ та ІІІ.
г) лише III та IV.
д) Тільки I, II та IV.
Відповідь: буква а).
II - Алкени - це сполуки з подвійним зв’язком, тобто ненасичені, але вони можуть мати наслідки у своєму ланцюзі, не будучи виключно лінійними.
IV - Бромметобензол та сполуки п-нітротолуолу належать до інших органічні функції.
Лайса Бернардес
Вчитель хімії
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/hidrocarbonetos.htm
