Розглянемо наступну хімічну рівновагу при постійній температурі:
3 години2 (г) + N2 (г) ↔ 2 NH3 (г)
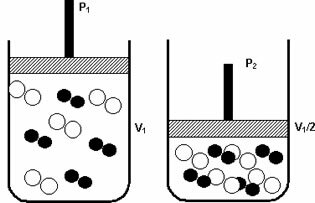
За словами Гей-Люссака, частка об'ємів газоподібних учасників реакції дорівнює співвідношенню відповідних стехіометричних коефіцієнтів. Простіше кажучи, можна сказати, що кількість молекул, присутніх у реагентах і продуктах, дорівнює коефіцієнтам у рівнянні.
У наведеному вище випадку в реагентах ми маємо 4 молекули, а в продуктах - 2 молекули, це означає, що об’єм реагентів більший, а об’єм продуктів менший.
Якщо ми збільшимо тиск у цій системі, баланс зміститься в бік меншого об'єму, щоб зменшити цей тиск. У випадку реакції, яку ми розглядаємо, витіснення відбуватиметься у прямому напрямку утворення продукту (NH3 (г)).
Однак, якщо ми зменшимо тиск, реакція рухатиметься до найбільшого об'єму у зворотному напрямку утворення реагентів (3 Н2 (г) + N2 (г)).
Не зупиняйтесь зараз... Після реклами є ще щось;)
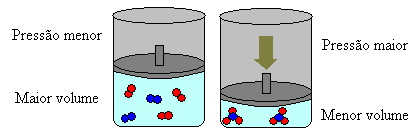
Це відбувається відповідно до Принципу Ле Шательє, який говорить, що будь-яке порушення (наприклад, зменшення або збільшення тиску) в системі в рівновазі змусить її рухатись у напрямку, що мінімізує це збурення, перенастроюючи себе до нового баланс.
Коротко, у випадку впливу зміни тиску на хімічну рівновагу можна сказати наступне:
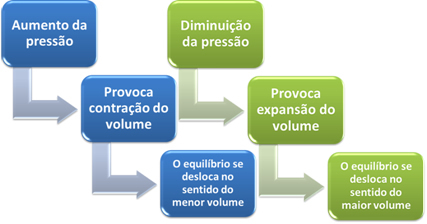
У разі реакцій, при яких об’єм реагентів дорівнює об’єму продуктів, хімічна рівновага не змінюється.
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Зміна тиску і зміщення хімічного балансу"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm. Доступ 28 червня 2021 року.
Хімія

Перевірте свої знання та дізнайтеся більше за допомогою цього списку розв’язаних вправ на хімічні баланси. Завдяки цьому матеріалу ви зможете краще зрозуміти, як працювати з константами рівноваги (Kp, Kc та Ki), зсувом рівноваги, pH та pOH, а також рівновагою в так званих буферних розчинах.