Вивчення сили a кислота дуже важливо для визначення здатності кислого розчину проводити електричний струм, оскільки це стосується кількості іонів, які ця речовина виробляє при контакті з водою (іонізація). Коли кислота занадто сильна, вона утворює занадто багато катіонів гідронію (H3О+) і багато аніонів (X-). Див. Рівняння іонізації бромистоводневої кислоти:
HBr + H2O → H3О+ + Br-
При іонізації водень, присутній у молекулі кислоти, взаємодіє з молекулою води і утворює гідроній. Але для того, щоб сталася ця подія, атом водню повинен бути обов’язково іонізуючим. Іонізуючий водень здатний утворювати катіон гідронію.. Щоб з’ясувати, чи є водень іонізуючим, ми беремо до уваги класифікацію кислоти як гідрацидної (не має кисню у своєму складі) чи оксикислоти (має кисень у своєму складі).
а) Гідрациди
Весь водень у гідрациді вважається іонізуючим.
Приклади:
- HCl: іонізуючий водень, утворюючи, таким чином, гідроній;
Не зупиняйтесь зараз... Після реклами є ще щось;)
- Ч.2S: Два іонізуються водню, отже, утворюються два гідрони
б) Оксикислота
В оксикислоті, іонізується лише водень, який зв’язаний з атомом кисню в молекулі. Для цього необхідно побудувати його структурну формулу. Див. Кілька прикладів:
H3ПИЛ4 (фосфорна кислота)
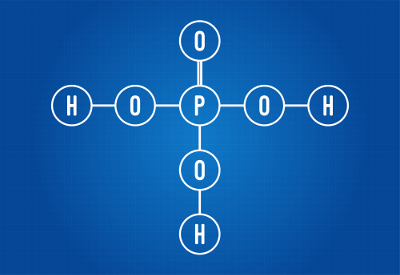
Структурна формула фосфорної кислоти
Ми бачимо, що у структурі фосфорної кислоти є три водню, зв’язані з киснем, отже, є три іонізуються водню. Рівнянням іонізації буде:
H3ПИЛ4 + 3 год2O → 3 H3О+ + PO4-3
H2ТІЛЬКИ4 (сірчана кислота)
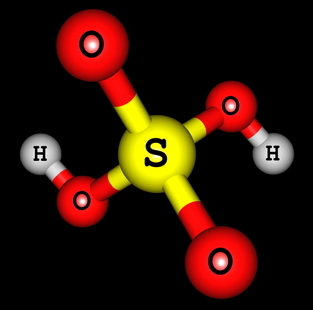
Структурна формула сірчаної кислоти
Ми бачимо, що в структурі сірчаної кислоти є два водню, зв’язані з киснем, тому є два іонізуються водню. Рівнянням іонізації буде:
H2ТІЛЬКИ4 + 2 год2O → 2 H3О+ + ОС4-2
Мені Діого Лопес Діас
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
ДНІ, Діоґо Лопес. «Іонізуючий водень»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm. Доступ 28 червня 2021 року.
Хімія

Дисоціація та іонізація, італійський вчений Вольта, електричний струм, шведський фізик-хімік Сван Август Арреніус, теорія Арреній, позитивні іони, катіони, негативні іони, аніони, їдкий натр, кухонна сіль, полярні молекули, дисоціація іонний,