Коли ми подаємо різні елементи дії полум’я, ми помічаємо, що кожен з них випромінює інший колір. Наприклад, якщо ми спалюємо стронцій, натрій та мідну сіль, ми побачимо, відповідно, червоний, насичений жовтий та зелений кольори, як показано на наступному малюнку:

Якщо світло від цього полум’я падає на призму, a розривний спектр, тобто лише кілька кольорових яскравих ліній будуть спостерігатися впереміш з регіонами без світла. Для кожного елемента ми матимемо різний спектр.

Ці типи спектрів називаються спектр випромінювання, оскільки вони були видані певним елементом і служать для його ідентифікації.
Отримати подібні спектри можна за допомогою світлового пучка, що виробляється в електророзрядної трубці на висоті температури та низького тиску, що містять гази певних елементів, таких як водень, або як благородні гази нижче:

Пропускаючи це електромагнітне випромінювання (світло), що виробляється крізь призму, отримують спектри випромінювання кожного з цих елементів.
Раніше вважалося, що отриманий сонячний спектр був абсолютно безперервним, але англійський вчений Вільям Гайд Волластон виявив, що до працюючи з дуже вузьким променем світла, з щілиною близько 0,01 мм, ви могли побачити, що сонячний спектр містив сім чорних ліній про це. Пізніше молоді
Йозеф Фраунгофер (1787-1826), використовуючи призми та дифракційні решітки, виявив, що сонячний спектр насправді містить тисячі накладених чорних ліній.Через деякий час фізичний Густав Роберт Кірхгофф він помітив, що жовті плями, досягнуті за допомогою натрієвого спектру, знаходились точно там же, де і дві чорні лінії в спектрі Сонця. він і хімік Роберт Вільгельм Бунзен здійснив кілька експериментів і помітив, що якщо біле світло від пальника Бунзена, таке як сонячне світло, проходить повз жовте світло, що випромінюється натрієм, і призму перетинається для створення спектру; результатом буде безперервний сонячний спектр у кольорах веселки, але з чорними лініями (які Фраунгофер називав лініями D) у тому ж положенні, що і жовті лінії в натрієвому спектрі.
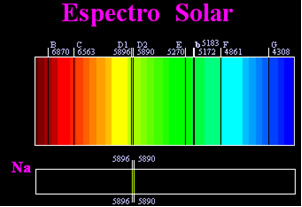
Сонце випромінює світло всіх кольорів, від червоного до фіолетового, однак, проходячи через атмосферу Землі, наявні гази поглинають світло Сонця саме в тих кольорах, які вони випромінюють.
Ці типи спектрів називаються спектри поглинання.
На основі цих спостережень, Кірхофф створили три закони для спектроскопії, які:
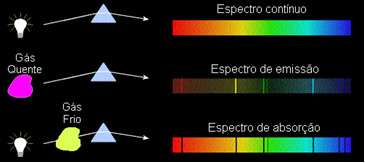
1) Тіло непрозорий гарячий, в будь-якому з трьох фізичних станів, випромінює спектр безперервний.
2) Газ прозорий - подібно до тих благородних газів, які ми бачили вище - виробляє спектр випромінювання, з появою ліній яскравий. Кількість і положення цих ліній визначатимуться хімічними елементами, присутніми в газі.
3) Якщо a безперервний спектр проходить через газ при найнижчій температурі холодний газ викликає присутність темні лінії, тобто a спектр поглинання. Так сталося із спектром сонячного світла, що проходить через газ натрію. У цьому випадку кількість і положення ліній в спектрі поглинання також залежать від хімічних елементів, що присутні в газі.
Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm
