Ефір це киснева органічна функція, тобто вона має хімічний елемент кисень, крім вуглецю та водню. Ця функція має основною структурною характеристикою наявність двох органічні радикали приєднаний до атома кисню.
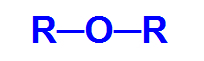
Загальна структурна формула ефіру
Таким чином, вуглецевий ланцюг ефіру неоднорідний і може мати два однакові або різні радикали алкіл, типи радикалів, що не мають ароматичної структури, або арил, радикали, які не мають структури ароматичний.
Фізичні характеристики ефіру
Що стосується фізичного стану при кімнатній температурі: коли ефір він має у своєму складі чотири і більше атомів вуглецю, він рідкий;
Що стосується температури плавлення та температури кипіння: якщо порівнювати з іншими масовими органічними сполуками приблизні моляри, мають температуру плавлення, подібну до температури алканів і нижчу, ніж решта сполук органічні;
Що стосується щільності: це сполуки, які мають малу щільність у порівнянні з водою;
Що стосується сил взаємодії: ефіри складаються з низькою полярністю, взаємодіючи між собою через слабку постійну дипольну взаємодію. З водою та спиртами ефіри мають здатність взаємодіяти за допомогою водневих зв’язків.
Що стосується полярність: - це сполуки, що мають кутову геометрію, отже, вони є полярними.
Що стосується органолептичної характеристики: це речовини, які видають дуже приємний запах, але їх вдихання може викликати залежність.
Офіційна номенклатура ефіру
Префікс другорядного стебла + окси + префікс головного стебла + інфікс + o
Здійснити офіційну номенклатуру a ефір, Дуже важливо визначити, який ваш головний ліганд, а який другорядний ліганд. Для цього дотримуйтесь двох прикладів застосування цього правила іменування нижче:
1-й приклад:
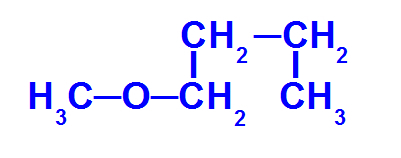
Структурна формула ефіру з меншою кількістю вуглецю
Ефір, наведений вище, має такі радикали:
Метил (СН3-);
Бутил (СН3-CH2-CH2-CH2-).
Щоб назвати цю сполуку, ми маємо:
незначний радикальний префікс: Met
+
окси
+
основний префікс стовбура: але
+
an (оскільки він має лише окремі посилання)
+
О
Отже, назва цього ефір це буде метоксибутан.
2-й приклад:
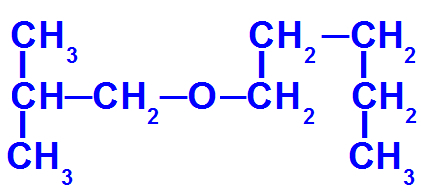
Структурна формула ефіру з більшою кількістю вуглецю
Цей ефір має такі радикали:
Ізобутил [(СН3)2-CH-CH2-);
пентил (СН3-CH2-CH2-CH2-CH2).
Отже, щоб назвати це, ми маємо:
незначний радикальний префікс: ізобут
+
окси
+
основний префікс стебла: pent
+
an (оскільки він має лише окремі посилання)
+
О
Таким чином, назва ефір йдеться про ізобутоксипентан.
Звичайна номенклатура ефіру
Ефір + назва радикалів (найпростіший, а потім найскладніший) + ico
або
Радикальні назви + ефір
Нижче наведено два приклади застосування цього правила іменування:
1-й приклад:

Структурна формула ефіру, який має чотири вуглеці
Це ефір представляє такі радикали:
Метил (СН3);
Ізопропіл (СН3-CH-CH3).
Отже, для цієї сполуки ми маємо:
Ефір
+
незначний радикал: Метил
+
основний радикальний префікс: ізопропіл
+
ich
Таким чином, назва ефір йдеться про метиловий ізопропіловий ефір, або ж про метиловий ізопропіловий ефір.
2-й приклад:

Структурна формула ефіру, що містить п’ять вуглеводнів
Ефір, наведений вище, має такі радикали:
Етил (СН3-CH2-);
Пропіл (СН3-CH2-CH2-).
Щоб назвати цю сполуку, ми маємо:
Ефір
+
незначний радикал: етил
+
основний радикальний префікс: пропіл
+
ich
Таким чином, назва ефір йдеться про етиловий пропіловий ефір, який також може бути етиловий пропіловий ефір.
Використання ефірів
Загалом ефіри використовуються:
Як інертні органічні розчинники, тобто не беруть участі в жодній реакції;
Використовується при видобутку есенцій, таких як квіти, деревина тощо;
Використовується при видобутку різних масел і жирів.
Мені Діого Лопес
Джерело: Бразильська школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eter.htm

