О розрахунок атомна маса елемента - це математичний ресурс, який використовується для визначення величини маси, присутньої в Періодичній системі кожного з існуючих хімічних елементів. Загалом, проводити розрахунок атомної маси, ми повинні знати наступні змінні хімічний елемент:
Ізотопи елементів;
Масове число кожного ізотопу елемента;
Відсоток кожного ізотопу елемента в природі.
Наприклад, розрахунок атомної маси Гідрогену проводився на основі таких даних:
Представляє ізотопи проти (H1), дейтерій (H2) і тритію (H3);
Маси цих ізотопів становлять 1, 2 і 3 відповідно;
Відсоток Протію в природі становить 98,9%;
Відсоток дейтерію в природі становить 0,09%;
Відсоток тритію в природі становить 0,01%.
Математичний стандарт для обчислення атомної маси
Для проведення розрахунок атомної маси будь-якого хімічного елемента, ми повинні використовувати наступну математичну схему:
1О: помножте масове число кожного ізотопу на його відсоток;
2О: додати всі результати, знайдені в першому кроці множення;
3О: ділимо знайдену суму на 100.
M.A. = масове число. відсоток + масове число. відсоток
100
Карта розуму: атомна маса
* Щоб завантажити карту розуму у форматі PDF, Натисніть тут!
Приклади розрахунку атомної маси
⇒ 1-й приклад: Розрахунок атомної маси Сірки.
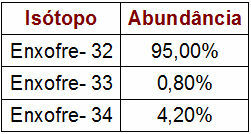
Дані про відсоток та масу ізотопів сірки
У наведеній таблиці вказано масове число та відсоток кожного ізотопу сірки в природі. Щоб виконати розрахунок атомної маси, просто виконайте такі дії:
1О Крок: помножте масове число кожного ізотопу на величину його чисельності.
Сірка - 32 (S32)
s32 = 32.95
s32 = 3040
Сірка - 33 (S33)
s33 = 33.0,8
s33 = 26,4
Сірка - 34 (S34)
s34 = 34.4,2
s34 = 142,8
2О Крок: додати значення, знайдені у множеннях масового числа та достатку ізотопу.
Сума = S32 + S33 + S34
Сума = 3040 + 26,4 + 142,8
Сума = 3209,2
3О Крок: обчислити атомну масу, поділивши суму знайдених результатів на 100:
M.A. = Сума
100
M.A. = 3209,2
100
M.A. = 32 092 од
⇒ 2-й приклад: Даний хімічний елемент (D) має три ізотопи, масові числа яких:
30D 32D 34D
Знаючи, що атомна маса цього елемента дорівнює 32,20 мкм, а ізотоп становить 20% 32D в природі, яке значення відсотків інших ізотопів?
У твердженні наводяться масові числа, атомна маса та відсоток одного з ізотопів. Щоб визначити відсоток інших ізотопів, ми повинні виконати наступні кроки:
1О Крок: визначити відсоток кожного ізотопу.
Ізотоп - 30 (DS30)
DS30 = 30.x
DS30 = 30x
Ізотоп - 32 (DS32)
DS32 = 32.20
DS32 = 640
Ізотоп - 34 (D34)
DS34 = 34.у
DS34 = 34р
2О Крок: використовувати всі дані, знайдені в математичному виразі, для обчислення атомної маси.
M.A. = масове число. відсоток + масове число. відсоток
100
32,2 = 30x + 640 + 34р
100
32,2.100 = 30x + 640 + 34р
100
3220 - 640 = 30x + 34р
30x + 34y = 2580
x = 2580 - 34р
30
3О Крок: використовуйте вираз, знайдений вище, з таких міркувань:
Відсоток ізотопу 1 + Відсоток ізотопу 2 + Відсоток ізотопу 3 = 100%
x + 20 + y = 100
x + y = 100-20
x + y = 80
x = 80 - y
2580 - 34р = 80-річний
30
2580 - 34y = 30. (80 років)
2580- 34 р = 2400 - 30р
2580 - 2400 = 34р-30р
4y = 180
y = 80
4
y = 45%
4О Крок: обчислити відсоткове значення x у виразі, побудованому на третьому кроці.
x + y = 80
х + 45 = 80
x = 80 - 45
х = 35%
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm
