THE ланцюгова ізомерія являє собою тип плоскої або конституціональної ізомерії, тобто два або більше сполук мають однакові молекулярна формула (однакові хімічні елементи та в однаковій кількості), але вони відрізняються за формулою структурна.
У разі ізомерії ланцюга (також її називають серцевинною ізомерією або скелетною ізомерією) сполуки належать до однієї і тієї ж органічної функції, але різниця полягає у типі ланцюга.
Наприклад, ми можемо мати такі випадки:
1 - Один ізомер може мати відкритий (ациклічний) ланцюг, тоді як інший має замкнутий (циклічний) ланцюг;
2 - Один ізомер може мати насичений ланцюг (лише одинарні зв’язки між вуглецями), тоді як інший ізомер ненасичений (має принаймні один подвійний зв’язок між вуглецями);
3 - Один має нормальний ланцюг, а інший має розгалужений ланцюг;
4 - Один має однорідний ланцюг, а інший - неоднорідний ланцюг.
Якщо у вас виникли запитання щодо таких типів вуглецевих ланцюгів, прочитайте текст Класифікація вуглецевих ланцюгів.
Тепер розглянемо кілька прикладів ланцюгової ізомерії:
1- Відкритий і закритий ланцюг:
Наступні ізомери мають молекулярну формулу С5H10, але вони відрізняються тим, що один має відкритий ланцюг, а інший - замкнутий ланцюг:

Ізомери ланцюга (відкриті та закриті)
Крім того, цей приклад також вписується в такий тип ізомерії ланцюга:
2- Насичений і ненасичений ланцюг:
У попередньому прикладі ми побачили, що ланцюг пент-1-ен ненасичений, оскільки він має подвійний зв'язок між двома вуглецями, тоді як циклопентан насичений, тобто він має лише поодинокі зв'язки.
Див. Інший приклад: Молекулярна формула: C3H6:
СН2 ═ СН ─ СН3 і СН2
/ \
H2C CH2
пропен циклопропан
Не зупиняйтесь зараз... Після реклами є ще щось;)
3- Звичайний і розгалужений ланцюг:
Цей тип ізомерії може зустрічатися в закритих або відкритих ланцюгах. Наприклад, циклопентан, показаний у першому пункті, не має гілок, але інший його ізомер, метилциклобутан, має. Подивіться:

Ізомери ланцюга (нормальні та розгалужені)
Тепер подивимось на приклад цього типу відкрито-ланцюгової ізомерії. Молекулярна формула таких ізомерів: C4H8О2:
H3C CH2 ─ СН2─ КООН і СН3 ─ CH ─ COOH
│
СН3
Бутанова кислота 2-метилпропанова кислота
4- Однорідний і неоднорідний ланцюг:
Однорідний ланцюг - це той, що має лише атоми вуглецю, тоді як гетерогенний ланцюг - той, що має а гетероатом, тобто атом якогось хімічного елемента між вуглецями, наприклад кисню, азоту, сірки та люмінофор.
Приклад: C2H7N:
H3C ─ N ─ СН3 та H3C CH2 ─ NH2
│
H
диметиламін етиламін
(неоднорідний) (однорідний)
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. «Ланцюгова ізомерія»; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/isomeria-cadeia.htm. Доступ 27 червня 2021 року.
Хімія
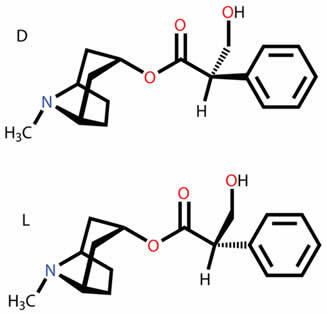
Знайте, що таке різні типи плоских та просторових ізомерів, такі як функція, положення, ланцюг, таутомерія, метамерія, цис-транс геометрична та оптична ізомерія.