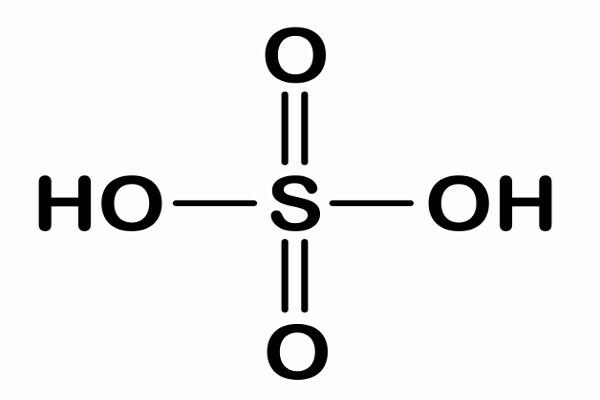
Karbonun değerlik kabuğunda dört elektronu vardır, yani dört bağ oluşturabilir, böylece diğer atomlara katılabilir. olarak: H, O, N, Cl. Karbonun sahip olduğu bu özellik, doğada bulunan organik bileşiklerin çeşitliliğini açıklar, bu nedenle karbonun dört değerlikli.
1874 yılında Van't Hoff ve Le Bel, karbon için uzaysal bir model yarattı. Bu model, düzenli tetrahedronlarla temsil edilen karbon atomlarına sahipti, karbon tetrahedronun merkezini işgal etti ve dört değerlik dört köşesine karşılık geldi.
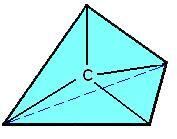
Karbonun uzaysal formülü.
Bu modelde, karbon atomları arasında meydana gelen farklı bağ türleri aşağıdaki gibi temsil edilmiştir:
) basit bağlantı - tetrahedronlar bir tepe noktası (tek bağ) ile bağlanır;


b) Çift bağ - tetrahedronlar iki köşe (bir kenar) ile birleştirilir;

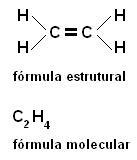
c) Üçlü bağlantı - tetrahedronlar üç köşe ile birleştirilir (bir yüz);
Şimdi durma... Reklamdan sonra devamı var ;)

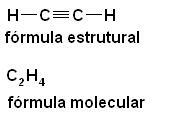
Atom modelinin evrimi, atomun bir çekirdeğe ve bir elektrosfere sahip olduğunu gösterdi ve bu da yeni modellerin ortaya çıkmasını sağladı. karbon tarafından yapılan bağları açıklamak için: 1915 yılında Lewis, atomların bağlanması için yeni bir öneri sundu. karbon. Lewis'e göre, değerlik katmanında atomlar elektronik çiftler aracılığıyla bağlanmıştır. Bu temsile Lewis Elektronik Formülü adı verildi ve atomların elektronik çiftler aracılığıyla birleştiği bağ türü kovalent bağ olarak bilinir.

Lewis Elektronik Formülü
Organik moleküllerin büyük çoğunluğu üç boyutludur, bu nedenle sadece yapıyı değil aynı zamanda geometriyi de gösteren modellerin kullanılmasına ihtiyaç vardır. Bu nedenle uzaysal formül karbonun yapısını anlamak için daha uygundur.
Líria Alves tarafından
Kimya mezunu
Brezilya Okul Takımı
Organik Kimya - Kimya - Brezilya Okulu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
SOUZA, Liria Alves de. "Karbon Yapısal Formüller"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/formulas-estruturais-carbono.htm. 28 Haziran 2021'de erişildi.