bu çözünürlük veya çözünürlük katsayısı, laboratuvarda her zaman pratik olarak belirlenen maddenin fiziksel bir özelliğidir. olarak adlandırılan bir malzemenin kapasitesi ile ilgilidir. çözünen, bir başkası tarafından çözülecek hediyeler, çözücü.
Çözünürlüğe gelince, çözünenler aşağıdaki gibi sınıflandırılabilir:
Çözünür: çözücüde çözünenler. Sodyum klorür (çözünen), örneğin suda (çözücü) çözünür;
Az çözünür: çözücüde çözünmekte zorluk çekenler. Kalsiyum hidroksit [Ca(OH) durumu budur.2] (çözünen) suda;
Çözünmeyenler: bunlar çözücüde çözünmezler. Örneğin kum (çözünen), suda çözünmez.
bu çözünürlük hazırlanması ile çok ilişkilidir. çözümler (homojen karışımlar), çünkü bir çözelti elde etmek için kullanılan çözünenin çözücü içinde çözünür olması esastır.
Çözünürlüğü etkileyen faktörler
Çözünen çözücü içinde çözünür olsa bile, çözünenin çözünme yeteneğini etkileyebilecek bazı faktörler vardır. Onlar:
a) Çözünen ve çözücü miktarı arasındaki ilişki
Çözücünün her zaman çözebileceği bir çözünen sınırı vardır. Çözünen miktarını korurken çözücü miktarını arttırırsak, çözücü kullanılan tüm çözünenleri çözme eğilimindedir.
B) Sıcaklık
Sıcaklık, belirli bir çözünen maddeye göre bir çözücünün çözünürlüğünü değiştirebilen tek fiziksel faktördür. Bu değişiklik, aşağıda göreceğimiz gibi, çözünenin doğasına bağlıdır:
endotermik çözünen: çözücü oda sıcaklığından daha yüksek bir sıcaklıkta olduğu sürece daha büyük bir kütleyi çözmeyi başardığımızdır. Çözücü ne kadar sıcak olursa, o kadar fazla çözünen çözülür.
Misal: Su sıcakken daha fazla miktarda çekilmiş kahveyi çözmek mümkündür.
Ekzotermik çözünen: çözücü oda sıcaklığından daha düşük bir sıcaklıkta olduğu sürece daha büyük bir kütleyi çözmeyi başardığımızdır. Çözücü ne kadar soğuk olursa, o kadar fazla çözünen çözülür.
Misal: Soda soğukken daha fazla miktarda karbondioksiti çözmek mümkündür.
Çözünürlüğü belirleme yolları
Çözünürlük deneysel bir şekilde belirlenen bir özellik olduğundan, malzemeler genel olarak çözünürlüklerini en farklı çözücülerde değerlendirilmiştir. Böylece, bir çözünenin belirli bir çözücü içindeki çözünürlüğüne aşağıdaki gibi erişebiliriz:
a) Bir tablonun analizi
Çoğu zaman, öğrenci bir tablonun yorumlanmasından çözünürlükle karşılaşabilir. Aşağıdaki örneğe bakın:
Misal: (UEPG - uyarlanmış) Aşağıdaki tablo Li tuzunun çözünürlüğünü göstermektedir.2CO3 100 gram su içinde.
Şimdi durma... Reklamdan sonra devamı var ;)

Tablo, Li'nin gram cinsinden kütle değerlerini sunar.2CO3 0'dan 100 gram suda çözülebilen ÖC ila 50 ÖÇ. Su ne kadar sıcaksa o kadar az Li olduğunu görebiliriz.2CO3 çözülür. Bu nedenle, Li2CO3 ekzotermik bir çözünendir (su soğuksa daha fazla çözülür).
b) Bir grafiğin analizi
Çözünürlük, bir grafik yorumlanarak değerlendirilebilir. Bunu yapmak için, sadece sıcaklığı belirleyin, eğriye çevirin ve ardından eğriyi, çözülecek çözünen maddenin gram cinsinden kütlesi olan y eksenine çevirin.
Misal: (UFTM - uyarlanmış) Grafik, bir AX tuzunun çözünürlük eğrisini gösterir2.
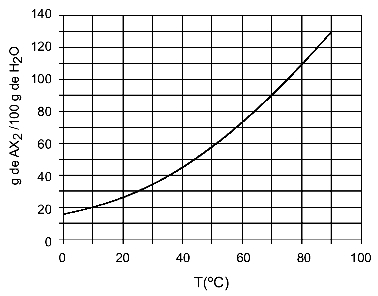
Grafik, y ekseninde su (çözücü) miktarının 100 gram olduğunu söylüyor. çözünen AX için2, su miktarını aşağıdaki sıcaklıklarda belirleyeceğiz:
30ÖÇ: Sıcaklığı açtığımızda 30ÖC eğrisine ve ardından y eksenine eğri, bu sıcaklıkta 100 gram su yaklaşık 35 gram çözünen AX'i çözebilir.2.
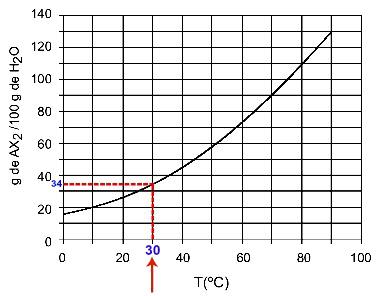
AX çözünürlüğünün belirlenmesi2 30 yaşındaÖÇ
40ÖÇ: Sıcaklığı açtığımızda 40ÖC eğrisine ve sonra y eksenine eğri, bu sıcaklıkta 100 gram su yaklaşık 45 gram çözünen AX'i çözebilir.2.
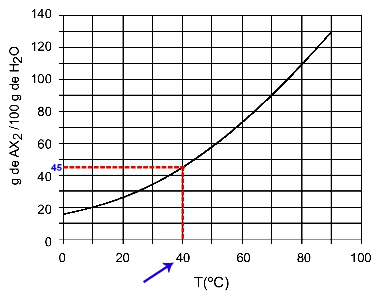
AX çözünürlüğünün belirlenmesi2 40 yaşındaÖÇ
Sıcaklıktaki her artışla çözünen madde miktarı daha büyük olduğundan, AX2 endotermik bir çözünendir.
c) metinsel yorumlama
Aşağıdaki örneğe bakın:
Misal: (PUC-MG) Bazı maddeler diğer maddelerle homojen karışımlar oluşturabilir. Miktarı en fazla olan maddeye çözücü, miktarı en az olana ise çözünen denir. Sodyum klorür (NaCl), su ile homojen bir çözelti oluşturur, bu çözelti içinde 20ºC'de 36 g NaCl'yi 100 g suda çözündürmek mümkündür.
Metin, eğer elimizde 100 gram su (çözücü) varsa, 20°C sıcaklıkta ÖC, 36 grama kadar NaCl'yi çözmek mümkündür.
Benden Diogo Lopes Dias
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
GÜNLER, Diogo Lopes. "Çözünürlük nedir?"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm. 28 Haziran 2021'de erişildi.