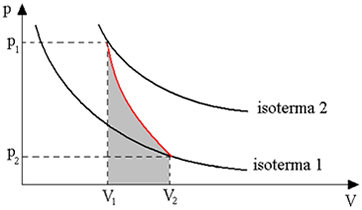
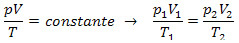Bir sıvıyı bir kapta bırakırsak, zamanla çıplak gözle görülmese bile hacminin azaldığını görürüz. Durgun sıvılarda gözlemleyebildiğimiz bir özellik, onları oluşturan parçacıkların önemli hareketlilik, bununla çekim güçlerinin üstesinden gelmeyi başarır ve böylece devlete geçerler. gazlı. Bu işlem, sıvının kaynama sıcaklığının altındaki herhangi bir sıcaklıkta gerçekleşir ve buharlaşma olarak adlandırılır.
tanımlayabiliriz buharlaşma parçacıkların sıvının yüzeyinden ayrılarak gaz haline geçtiği bir süreç olarak.
Vurgulamamız gereken ilginç bir gerçek, sıvıyı terk eden aynı parçacıkların sıvıya nüfuz ederek ilk duruma - bu durumda, yukarıdaki şekilde gösterildiği gibi sıvı durumuna - geri dönmesidir. Bahsedilen bu iki sürecin aynı anda gerçekleştiğini ve her zaman dengeye ulaşılarak iki fazın bir arada var olduğunu unutmamalıyız. Böylece, sıvının sıcaklığı ne kadar yüksek olursa, parçacıklarının hareketinin o kadar büyük olduğunu ve bununla birlikte daha fazla sayıda sıvının sıvıdan çıkacağını söyleyebiliriz.
Şimdi durma... Reklamdan sonra devamı var ;)
bu Buhar basıncı sıvıyı terk eden parçacıkların sıvının, daha doğrusu kabın yüzeyine uyguladıkları basınçtan başka bir şey değildir. Sürecin tersine gerçekleşebileceğini, yani sıvının sıcaklığı düştüğünde gaz moleküllerinin bir kısmının sıvı hale dönebileceğini vurgulamak önemlidir.
tanımlayabiliriz denge buhar basıncı gaz ve sıvı fazların bir arada dengede bulunduğu faz olarak. Buharlaşma herhangi bir sıcaklık koşulunda gerçekleşir, ancak Tutar Oluşan gazın miktarı sıcaklığa bağlıdır. Buhar basıncı sıcaklığa bağlıdır.
Domitiano Marques tarafından
Fizik Mezunu
Brezilya Okul Takımı
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
SILVA, Domitiano Correa Marques da. "Buhar basıncı ve buharlaşma"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/fisica/pressao-vapor-evaporacao.htm. 27 Haziran 2021'de erişildi.