Joseph Lous Gay-Lussac (1778-1850), gazlarla ilgili önemli çalışmalar yapan bir bilim adamıydı. Hidrojen ve oksijen gazları arasındaki reaksiyondan su üretimini gerçekleştirdi ve bunların doğru olduğunu doğruladı. her zaman iki hacim hidrojenin bir hacim oksijene oranında reaksiyona girerek iki hacim hidrojen üretir. Su:
Hidrojen + Oksijen → Su
1. Deney: 2 L 1 L 2 L
2. Deney: 4 L 2 L 4 L
3. Deney: 8 L 4 L 8 L
4. Deney: 16 L 8 L 160 L
Tüm deneylerde oranın her zaman aynı olduğuna dikkat edin: 2: 1: 2.
Birkaç deney ve analizden sonra, aynı şeyin gazlar arasındaki diğer reaksiyon türlerinde, yani reaksiyonlarda meydana geldiğini fark etti. her zaman sabit bir hacim oranı izledi, bu bilim adamı olarak bilinen gaz halindeki hacimlerdeki reaksiyonların aşağıdaki yasasına ulaştı: Gay-Lussac Hacim Yasası veya Hacimlerin Kombinasyonu Yasası:

Gay-Lussac'ın hacimsel yasasının ifadesi
Ama bu yasaya aykırıydı. Dalton'un atom teorisi, her şeyin büyük ve bölünmez küresel parçacıklardan, atomlardan oluştuğunu söyledi. Bu teoriye göre, reaksiyondaki ürünlerin hacmi, tepkenlerin hacimlerinin toplamına eşit olmalıdır. Bu nedenle, aşağıdakiler gerçekleşmelidir:
Hidrojen + Oksijen → Su
2 cilt + 1 cilt → 3 cilt
Ancak Gay-Lussac, pratikte durumun böyle olmadığını, sonucun iki hacim su buharına eşit olduğunu gösterdi.
Bu bariz çelişkinin cevabı, hipotez veya Avogadro yasası.

İtalya'da basılan damga Amedeo Avogadro'yu ve onun kanununun 1956'da ilan edilişini gösteriyor*
Amedeo Avogadro (1776-1856), gerçekte gazların izole edilmiş atomlar değil, moleküller olduğunu gösterdi. soy gazlar). Onun kanunu dedi ki:

Avogadro Yasası Açıklaması
Avogadro gösterdi ki 1 mol Herhangi bir gazın 6.02'si vardır. 1023 moleküller. Bu değer olarak bilinir Avogadro sayısı veya sabiti. Basıncın 1 atm ve sıcaklığın 273 K (0°C) olduğu Normal Sıcaklık ve Basınç Koşullarında (CNTP), 1 mol gazın kapladığı hacim her zaman 22,4 L olacaktır. Bu değer şuna karşılık gelir: gazların molar hacmi. Bu ilişkiler, alıştırmaları çözmek için çok önemlidir. stokiyometri.
Bu garip görünebilir, çünkü şu soru akla gelebilir: Molekülleri ve farklı büyüklüklerdeki atomları olan gazlar nasıl aynı hacmi kaplayabilir?
Bunun nedeni, gaz moleküllerinin birbirinden o kadar uzak olmasıdır ki, moleküllerin boyutu ihmal edilebilir.
Avogadro'nun hacim yasası bu şekilde Gay-Lussac'ın hacim yasasını açıkladı. Aşağıda, iki hidrojen molekülünün (iki hacim) bir oksijen molekülü (bir hacim) ile reaksiyona girerek iki su molekülü (iki hacim) oluşturduğuna dikkat edin. Su ve hidrojen, Avogadro yasasında belirtildiği gibi, aynı miktarda moleküle sahip oldukları için aynı hacme sahiptir.
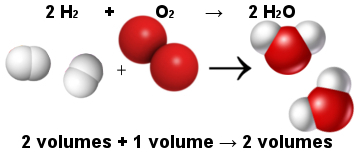
Su oluşum reaksiyonunda moleküller arasındaki oran
Aynı zamanda, Avogadro yasası atom teorisini ayakta tuttu, gördüğünüz gibi hem reaktanlarda hem de ürünlerde toplam 6 atom (4 hidrojen ve 2 oksijen) var.
Bu hacimsel yasalar, hacim kavramının gelişimi için çok önemliydi. moleküller.
* Telif hakkıyla korunan görsel: kale 76 / Shutterstock.com
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/lei-volumetrica-gay-lussac.htm


