Hücreler veya elektrokimyasal hücreler ve piller, kimyasal enerjinin kendiliğinden elektrik enerjisine dönüştürüldüğü cihazlardır..Hücre sadece iki elektrot ve bir elektrolitten oluşurken, pil seri veya paralel bir dizi pildir.
at birincil piller şarj edilemeyen cihazlardır, çünkü içlerinde meydana gelen oksidasyon-redüksiyon reaksiyonu durduğunda atılmaları gerekir.
Her ekipman için bir pil türü belirtilir ve şu anda kullanılan birincil piller arasında başlıcaları şunlardır: Leclanché kuru piller (ortak piller veya asit piller), alkali piller ve lityum/manganez dioksit piller.
Onları neyin farklı kıldığını ve hangi ekipman için uygun olduklarını görün:
- Leclanché Kuru Hücreler:
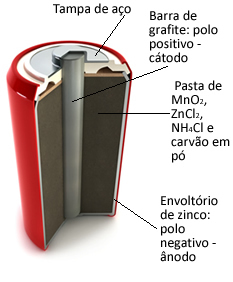
Bu yığınlar temel olarak, gözenekli bir kağıt ve manganez dioksit (MnO) ile çevrili merkezi bir grafit çubukla ayrılmış bir çinko zarftan oluşur.2), toz kömür (C) ve amonyum klorür (NH) içeren ıslak bir macun4Cl), çinko klorür (ZnCl2) ve su (H2Ö).
Ö çinko gibi çalışır anot, elektron kaybetmek; bu grafit gibi çalışır katot, elektronları manganez dioksite iletmek:
Anot Yarı Reaksiyonu: Zn (ler) → Zn2+(İşte) + 2 ve-
Katot Yarı Reaksiyonu: 2 MnO2(sulu) + 2 NH41+(İşte) + 2e- → 1 Dakika2Ö3(ler) + 2NH3(g) + 1 saat2Ö(1)
Küresel Reaksiyon: Zn (ler) + 2 MnO2(sulu) + 2 NH41+(İşte) → Zn2+(İşte) + 1 Milyon2Ö3(ler) + 2NH3(g)
Bu pil türü, uzaktan kumanda, duvar saati, taşınabilir radyo ve oyuncaklar gibi hafif ve sürekli deşarj gerektiren ekipmanlar için uygundur.
Bu pillerin çıkış noktası, işleyişi, dayanıklılığı, ddp, tehlikeleri ve alınması gereken önlemler hakkında daha detaylı bilgiyi yazıdan alabilirsiniz.Leclanché Kuru Yığın”.
Şimdi durma... Reklamdan sonra devamı var ;)
- Alkalin piller:
Çalışması Leclanché kuru hücrelerininkine çok benzer, ancak tek fark klorür yerine amonyum (asidik bir tuzdur), esas olarak sodyum hidroksit (NaOH) veya potasyum hidroksit (KOH) olmak üzere güçlü bir baz eklenir.
Anot Yarı Reaksiyonu: Zn + 2 OH → ZnO + H2O + 2e-
Katot Yarı Reaksiyonu: 2 MnO2 + H2O + 2e-→ Milyon2Ö3 + 2OH
Genel reaksiyon: Zn +2 MnO2→ ZnO + Mn 2Ö3

Alkalin piller, daha dayanıklı olmaları açısından asitli pillere göre daha avantajlıdır. tipik olarak aynı boyuttaki sıradan bir pilden %50-100 daha fazla güç sağlar, ayrıca daha az tehlike vardır sızıntılar.
Bunlar esas olarak radyolar, taşınabilir CD/DVD ve MP3 çalarlar, el fenerleri, dijital kameralar vb. gibi hızlı ve daha yoğun indirme gerektiren cihazlar için endikedir.
Ayrıca metni okuyun Alkalin piller.
- Lityum/manganez dioksit piller:
Bu piller hafiftir ve büyük bir voltaj (yaklaşık 3.4 V) üretir, bu nedenle genellikle saatler ve hesap makineleri gibi küçük ekipmanlarda kullanılırlar. Önceki durumlardan farklı olarak, aşağıdaki resimde gösterildiği gibi biçimi madeni paradır:

Anot lityumdur, katot manganez dioksittir ve elektrolit bir tuzlu su çözeltisidir:
Anot Yarım Reaksiyonu: oku →oku+ + ve−
Katot Yarı Reaksiyonu: MnO2 + oku+ + ve−→MnO2(li)
Genel tepki: Li + MnO2 → MnO2(li)
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "En Yaygın Hücre Tipleri ve Birincil Piller"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/tipos-pilhas-baterias-primarias-mais-comuns.htm. 27 Haziran 2021'de erişildi.
