inorganik tuzlar en az bir katyonun (herhangi bir metal veya amonyum tarafından oluşturulan) ve bir anyonun (basit veya bileşik) iyonik birleşimi ile oluşturulurlar.
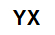
Bir tuzun genel moleküler formülü
Suya eklendiğinde, tuzlar ayrışır ve hidronyum dışında en az bir katyon (H+) ve hidroksit (OH) dışında bir anyon-).
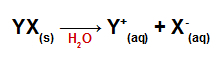
Herhangi bir tuz için ayrışma denklemi
Tuzların sınıflandırılması
Tuzlar genel olarak aşağıdaki sınıflandırmalara sahip olabilir:
basit tuz: Sadece bir katyon ve bir anyonun oluşturduğu tuz. Örnekler: NaCl, CaSO4, KCN, NH4CO3 vb.
Hidrojene tuz: iki katyonu (biri hidronyum olmalıdır) ve bir anyonu vardır. Örnekler: NaHCO3, CaHBO3 vb.
Hidroksil tuzu: bir katyonu ve iki anyonu vardır (bunlardan biri hidroksit olmalıdır). Örnekler: MgOHCl, Al(OH)2ClO3 vb.
Hidratlı tuz: kristal yapısıyla ilişkili su moleküllerini sunar. Örnekler: CaCl2.2H2O, CuSO4.6H2vb.
Çift tuz: iki katyonu (tümü hidronyumdan farklıdır) ve bir anyon veya bir katyon ve iki anyon (tümü hidroksitten farklıdır) vardır. Örnekler: Tür4CN, AgFeBO3 vb.
şap: +1 ve +3'e eşit NOx katyonlarına sahip iki sülfat artı 24 su molekülünün oluşturduğu tuzdur. Örnekler: Ag2SADECE4.Al2(SADECE4)3.24H2o, hayır2SADECE4.Sb2(SADECE4)3.24H2Ö
Tuz adlandırma kuralı
Anyon adı + de + katyon adı
→ K3TOZ4
Tuzun fosfat anyonu vardır (PO4-3) ve potasyum katyonu (K+1), dolayısıyla adı potasyum fosfattır.
→ Kasa3
Tuz, sülfit anyonuna sahiptir (SO3-2) ve kalsiyum katyonu (Ca+2), dolayısıyla adı kalsiyum sülfittir.
NOT: Katyon gümüş, çinko veya IA, IIA ve IIIA ailelerine ait bir element değilse, katyon adının önüne bir romen rakamı ile NOX'ini belirtmeliyiz.
→ Bakır2SADECE4
Tuz sülfat anyonuna sahiptir (SO4-2) ve kalsiyum katyonu (Cu+1), dolayısıyla adı bakır sülfat I'dir.
Hidrojene tuz: Bu tuz için anyon adından önce formüldeki hidrojen miktarına atıfta bulunan önek yazmalıyız. Bu önek kelimeden ayrı olmalıdır hidrojen bir kısa çizgi ile.
→ NaHCO3
Tuzun bir hidrojen, karbonat anyonu ve sodyum katyonu vardır, bu nedenle adı sodyum monohidrojen karbonattır.
Hidroksil tuzu: Bu tuz için anyon adından önce formüldeki hidroksil miktarına atıfta bulunan önek yazmalıyız. Bu önek kelimeden ayrı olmalıdır hidroksi bir kısa çizgi ile.
→ Al(OH)2ClO3
Tuzun iki hidroksil, klorat anyonu ve alüminyum katyonu vardır, dolayısıyla adı alüminyum dihidroksiklorattır.
Hidratlı tuz: Bu tuz için katyon adından sonra formüldeki su molekülü miktarına atıfta bulunan ön eki yazmalıyız. Bu önek kelimeden ayrı olmalıdır sulu bir kısa çizgi ile.
→ CaCl2.2H2Ö
Tuzun iki su molekülü vardır, klorür anyonu ve kalsiyum katyonu, dolayısıyla adı kalsiyum klorür dihidrattır.
İki katyonlu çift tuz: Bu tuz için anyon adından sonra parantez içinde çift kelimeyi ve ardından en elektropozitif katyon adını ve diğer katyonu yazmalıyız.
→ AgFeBO3
Bu tuz, borat anyonuna ek olarak gümüş (daha elektropozitif katyon) ve demir II katyonuna sahiptir. Adı borat (çift) gümüş ve demir II.
-
İki anyonlu çift tuz:
En elektronegatif anyonun adı + kısa çizgi + en az elektronegatif anyonun adı + de + katyon adı
→ Tür4CN
Bu tuz, fosfata (daha elektronegatif anyon) ve siyanür anyonuna ek olarak titanyum IV katyonu içerir. Adı titanyum siyanür fosfat IV'tür.
Şap tuzu: Bu tuz için genel kuralı görmezden geliyoruz. Şap terimini sırasıyla +3 yük katyon adını ve +1 yük katyon adını e bağlacı ile ayırarak yazın.
→ İçinde2SADECE4.Sb2(SADECE4)3.24H2Ö
Şap tuzu, +3 antimon katyonuna ve +1 sodyum katyonuna sahiptir, bu nedenle adı antimon III şap ve sodyumdur.
Tuzların fiziksel özellikleri
Oda sıcaklığında katıdırlar;
Yüksek erime ve kaynama noktalarına sahiptirler;
İyonik bağlardan oluşurlar;
Sıvı halde (füzyondan sonra) veya suda çözündüklerinde bir elektrik akımı iletirler;
Genel olarak, suda çözünürler, ancak pratik olarak çözünmez olarak kabul edilen tuzlar da vardır.
Tuzların kimyasal özellikleri
Tuzlar, birkaç madde grubuyla (başka bir maddeyle aynı katyona veya aynı anyona sahip olmamaları koşuluyla) kimyasal olarak reaksiyona girme yeteneğine sahip bileşiklerdir:
Bir asitle çift değişim reaksiyonunda: yeni bir tuz ve yeni bir asit oluştururlar.
Bir bazla çift değişim reaksiyonunda: yeni bir tuz ve yeni bir baz oluştururlar.
İçinde başka bir tuzla çift değişim reaksiyonu: iki yeni tuz oluşturur.
Bazı tuzlar acı çekme yeteneğine sahiptir. ayrışma ısıya maruz kaldığında iki veya daha fazla yeni madde oluşturur. Sodyum bikarbonatı (NaHCO) ısıtırsak3), örneğin, sodyum karbonat (Na) oluşturarak ayrışır.2CO3), su (H2O) ve karbondioksit (CO2).
Benden Diogo Lopes Dias
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-sais-inorganicos.htm

