bu sp-tipi karbon hibridizasyonu sadece iki pi bağı (π) ve iki sigma bağı (σ) oluşturduğunda olur. Bu durumda, iki olasılık vardır: karbon, aşağıda gösterildiği gibi iki çift bağ veya bir tek ve bir üçlü bağ yapabilir:
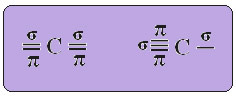
Metin "sp tipi hibridizasyon3” karbon hibridizasyonunun nasıl gerçekleştiğini ayrıntılı olarak gösterir. Hatırlama: hibridizasyon, birbirine eşdeğer, ancak orijinal saf orbitallerden farklı hibrit atomik orbitaller oluşturan saf atomik orbitallerin “karıştırılmasıdır”. Bu, başlangıçta şu şekilde temsil edilen karbon orbitallerinde olur:
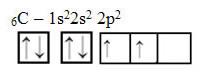
Bununla birlikte, enerjinin alınmasıyla, 2s orbitalinden bir elektron (bir okla gösterilir) 2p orbitaline yükseltilir:
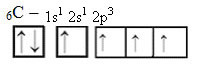
Bu şekilde, karbon, sadece iki değil, dört kovalent bağ yapabilen, eşleşmemiş dört yörüngeye sahiptir.
sp tipi hibridizasyon durumunda iki bağın pi olacağını biliyoruz; bunlar saf “p” orbitallerinde meydana gelirken, sp hibritleri olan diğer iki orbital, kalan sigma bağlarını yapacaktır.
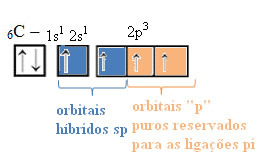
Bir hibrit sp orbitaline yol açan bir s ve bir p orbital arasındaki bu hibridizasyonun uzaysal temsili aşağıdaki gibi temsil edilebilir:
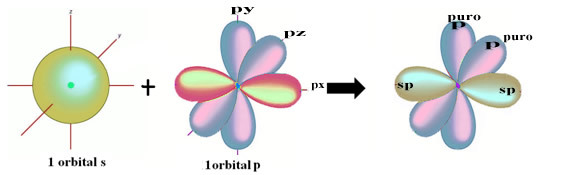
Yukarıdaki şekilde, pi bağlarını oluşturacak iki saf yörünge olduğu çok açıktır.
Bunun nasıl olduğunu anlamanız için, Amerika Birleşik Devletleri'nde ölüm cezasına çarptırılan mahkumlar için gaz odalarında kullanılan bir molekül siyanür gazı (HCN) örneğini ele alalım. Yapısal formülü şu şekilde verilir:
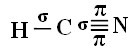
Karbona gelince, atomik orbitalleri zaten gösterildi, şimdi hidrojen ve nitrojen orbitallerine bakın:
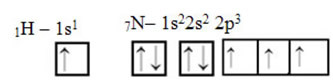
Sigma bağını gerçekleştirecek eşleşmemiş hidrojen yörüngesinin, uzaysal olarak bir daire ile temsil edilen “s” olduğuna dikkat edin; ve nitrojen orbitalleri, üç çift oval (her biri bir uzaysal alanda: x, y, z) ile temsil edilen “p” tipindedir. Böylece, HCN molekülünün yapısı aşağıdaki gibi temsil edilir:
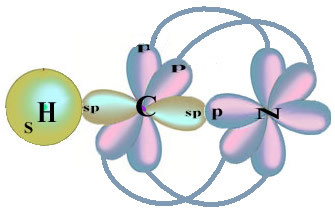
Bu formaldehit yapısında bulunan bağların türüne gelince:
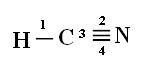
Bağlantılar: 1 = σs-sp
2 = σp-sp
3 = 4 = πp-p
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp.htm
