Enerji oksidasyonu alkinler ile asidik bir çözeltiye bir alkin (iki karbon arasında üçlü bağa sahip bir hidrokarbon) eklendiğinde meydana gelen organik bir reaksiyondur. reaktifi bayer (Potasyum Permanganat - KMnO4).
NOT: Bir reaksiyon enerji oksidasyonu potasyum dikromat (K2cr2Ö7) ve sadece potasyum permanganat değil.
Ne zaman bir tepki alkinlerde enerjik oksidasyon gerçekleştirilir, kaynaklanabilecek ürünler karboksilik asitler, su (bunlardan herhangi birinde görünen tek madde) ve karbondioksit (CO2).
Asidik ortamda Baeyer Reaktifi
Baeyer reaktifi su ile karıştırıldığında, asit (H iyonlarını serbest bırakabilen madde+), iki oluşumu var oksitler (potasyum oksit ve manganez oksit II) ve yeni oluşan oksijenler ([O]).

Alkinlerde enerji oksidasyonu mekanizmaları
1. Mekanizma: üçlü bağı kırmak.
Başlangıçta, üçlü bağ, Baeyer reaktifi tarafından oluşturulan yeni oluşan oksijenler tarafından saldırıya uğrar. Bu saldırı üçlü bağın tamamen kırılmasına neden olur.
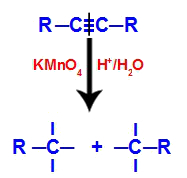
Oluşan oksijenlerin saldırısı ile üçlü bağın bozulması
Üçlü bağ kırıldığında alkin ikiye ayrılır. Üçlü bağ yapan karbonların her birinde üç serbest değerlik görünür.
2. Mekanizma: Hidroksil gruplarının etkileşimi
Üçlü bağın bulunduğu karbonlardaki serbest değerlerin her biri, bir poliol oluşturan hidroksil grupları (OH) tarafından işgal edilir (alkol birkaç hidroksil ile).
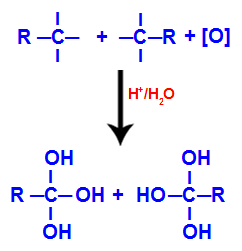
Üçlü bağ bölünmesinden sonra hidroksil gruplarıyla poliol oluşumu
NOT: Eskiden üçlü bağın bulunduğu karbonun kendisine bağlı bir hidrojen atomu varsa, bu hidrojen atomu yeni oluşan bir oksijen alacak ve ayrıca başka bir hidroksil oluşturacaktır.
3. Mekanizma: Su moleküllerinin oluşumu
Bir karbon iki veya daha fazla OH grubuna sahip olduğunda, aşırı derecede varlığından dolayı çok kararsız bir yapı haline gelir. elektronegatifler. Bu nedenle, kararsızlık nedeniyle molekül kendi kendine dehidrasyona uğrar, yani bir hidroksil hidronyuma bağlanır (H+) başka bir hidroksilden su oluşturur.

Oluşan poliolde bulunan iki hidroksilden su moleküllerinin oluşumu
4. Mekanizma: Ürün oluşumu
Su moleküllerinin oluşumundan sonra, karbonun çıkışı nedeniyle karbon bir bağ kaybeder. hidroksil ve diğer hidroksilin oksijeni de bir hidrojen. Bu nedenle, bu karbon ve oksijen arasında, bir karbonil (C=O) oluşturan ve her ikisini de stabilize eden bir çift bağ ortaya çıkar.
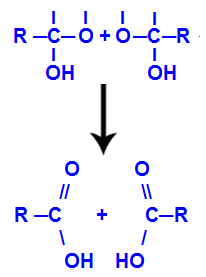
Alkinden elde edilen iki yapıda karbonil oluşumu
Alkin Enerjisi Oksidasyon Denklemi Örneği
Misal: But-1-ino'nun enerjik oksidasyonu
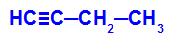
But-1-yne'nin yapısal formülü
But-1-yne, Bayer reaktifi, su ve asit içeren bir ortama yerleştirildiğinde, bağ kopar. denklemde olduğu gibi, ortada bulunan yeni oluşan oksijenlerin saldırısı nedeniyle karbon 1 ve 2 arasında bulunan üçlü feryat:
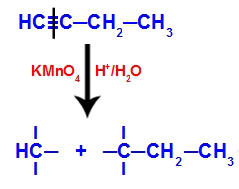
But-1-yne bağlantılarının kopması
Üçlü bağ kırıldıktan sonra karbon 1 ve 2 üç hidroksil alır, ancak karbon 1 bir tane daha alır çünkü iki poliol (parça 1 ve 2) oluşturan bir hidrojen atomuna (olmakta olan bir oksijene bağlanan) sahipti.

Poliollerin oluşumunu temsil eden denklem
Kısa bir süre sonra, polioller kararsız olduklarından, hidroksillerden su moleküllerinin oluşumuna sahibiz. 1. fragmanda bir su molekülü görünür (çünkü üç hidroksil vardır) ve 2. fragmanda iki molekül görünür (çünkü dört hidroksil vardır).
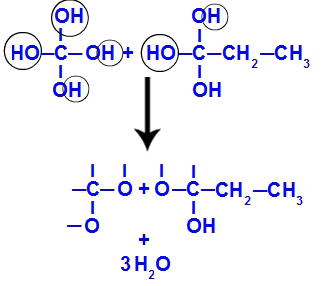
But-1-yne parçalarından su moleküllerinin oluşumu
Son olarak, hidroksil kaybeden karbonlar ile hidrojeni kaybeden oksijenler arasında karbonillere yol açan çift bağın oluşumuna sahibiz.

But-1-yne fragmanlarında karbonil oluşumu
Yukarıdaki denklemle, but-1-yne'nin bir karboksilik asit ve karbon dioksite (CO2) yol açtığını görebiliriz.2).
Benden Diogo Lopes Dias
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcinos.htm
