Halojenasyon reaksiyonları, bir tür organik ikame reaksiyonudur, yani içinde bir atom veya atom gruplarının başka bir molekülün atomları veya atom gruplarıyla yer değiştirmesi organik.
Genellikle bu tip reaksiyon alkanlar ve aromatik hidrokarbonlar (benzen ve türevleri) ile gerçekleşir.
Halojenasyon, halojenlerin basit maddelerinde meydana geldiği için bu adla anılır: F2, Cl2, br2 Hey2. Ancak bunlar arasında en yaygın olanı klorlamadır (Cl2) ve brominasyon (Br2), çünkü flor çok reaktiftir ve reaksiyonları patlayıcıdır ve organik maddeleri yok ederek bile kontrol edilmesi zordur:
CH4 (g) + 2 F2(g) → C(ler) + 4HF(g)
İyot ile reaksiyonlar son derece yavaştır.
Aşağıda ana halojenasyon türleri ve bazı örnekler verilmiştir:
1. Alkanlarla halojenasyon: Alkanlar zayıf reaktif olduklarından, halojenleşme reaksiyonları sadece güneş ışığı (λ), morötesi ışık veya güçlü ısıtma varlığında gerçekleşir. Bu tip reaksiyon, bir alkil halojenür elde etmek için yapılır.
Örnek: metan monoklorlama:
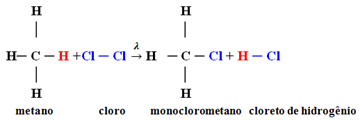
Bu durumda metan hidrojen atomundan (CH
4) monoklorometan veren bir klor atomu ile değiştirilir. Çok fazla klor varsa, bu reaksiyon metan içindeki tüm hidrojenleri değiştirerek işlemeye devam edebilir.1.1. 3'ten fazla karbon içeren alkanlarda halojenasyon: Reaksiyona girecek alkan en az 3 karbon atomuna sahipse, farklı ikame edilmiş bileşiklerin bir karışımı ile sonuçlanırız. Aşağıdaki metilbütan monoklorinasyon örneğine bakın:
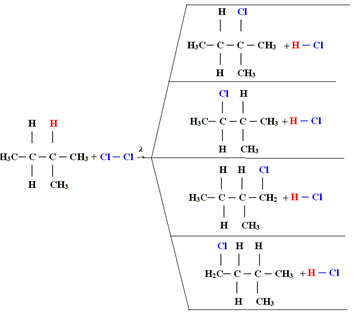
Her bileşiğin miktarı, hidrojenin moleküle salındığı aşağıdaki kolaylık sırası ile orantılı olacaktır:

Dolayısıyla yukarıdaki durumda en büyük miktar 2-metil-2-klorobütan ve en küçük miktar 2-metil-1-klorobütan olacaktır.
2. Benzen Halojenasyonu: Benzen normalde klor veya brom ile reaksiyona girmez. Bununla birlikte, katalizör olarak bir Lewis asidi kullanılıyorsa (genellikle FeCl3, FeBr3 veya AlCl3tümü susuz formda), benzen bir halojenasyon reaksiyonunda kolayca reaksiyona girer.
Klorür ve ferrik bromür, karışıma sadece demir eklenerek elde edilebilir ve bu şekilde halojen ile reaksiyona girer ve Lewis asidini üretir:
2 Fe + 3 Br2 → 2 FeBr3
Benzen halojenasyonuna ve mekanizmasına ilişkin bir örneğe bakın:
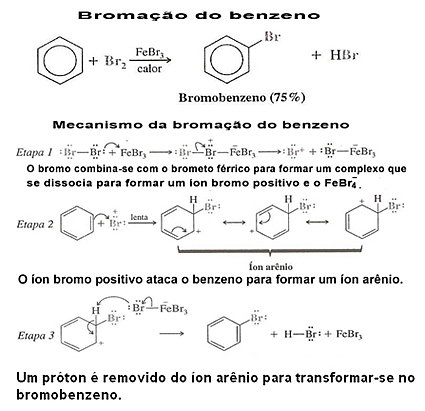
3. Benzen türevlerinin halojenasyonu:Bu durumlarda, ikame aromatik çekirdeğe bağlı olan ikame edici veya fonksiyonel grup tarafından yönlendirilir. Bunun nasıl olduğunu görmek için metinleri okuyun "Benzen Halkasındaki Direksiyon Radikalleri" ve "Meta ve orto-yönetmen radikallerinin elektronik etkileri”.
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm
