Sen bazik oksitler su ile reaksiyona girdiğinde bazlara yol açanlardır. Bir asitle tepkimeye girdiklerinde tuz ve su oluştururlar.
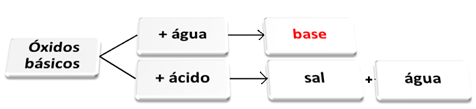
Su ve asit ile reaksiyona giren bazik oksitler.
Örneğin, sodyum oksitimiz var (Na2O), bir bazik oksittir. Aşağıya bakın, suyla reaksiyona girdiğinde sodyum hidroksit bazı oluşturur:
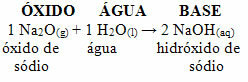
Aynı oksit, sülfürik asit gibi bir asitle reaksiyona girerse (H2BİR TEK4), bir tuz (sodyum sülfat) ve su üretilecektir.
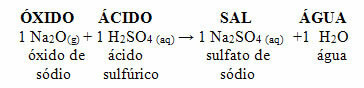
Bir bazik oksit, asidik bir oksit ile reaksiyona girerse, su olmadan bir tuz da üretilir.
Gösterilen örnekte gösterildiği gibi, diğer bazik oksitler de kendi hallerinde oluşan iyonik bileşiklerdir. çoğunlukla metaller tarafından, yüksek düzeyde elektropozitif olan, normalde +1'e eşit bir "yük" sunan elementler veya +2.
Örnekler:
NS2O = Na1+
K2O = K1+
CaO = Ca2+
MgO = Mg2+
Bu bileşikler yüksek erime ve kaynama noktalarına sahiptir ve hepsi oksijen anyonunu (O2-).
Bazı bazik oksitlerin uygulamaları:
• Köpek: Kalsiyum oksit
Bu bileşik yaygın olarak bilinir sönmemiş kireç. Su ile reaksiyona girdiğinde aşağıdaki reaksiyona göre duvarları boyamak için kullanılan bir baz (kalsiyum hidroksit) oluşur, böcekleri kovmak, mührü korumak ve sızmayı önlemek amacıyla ağaç gövdeleri ve diğer malzemeler sudan. Bu oluşan tabana denir.
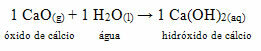

Badana boyama.
• K2Ö: potasyum oksit
Potasyum oksit genellikle odun ve sigara külünde bulunur. Su ile reaksiyona girdiğinde sabun üretiminde kullanılan baz potasyum hidroksiti (KOH) oluşturur. Geçmişte bile KOH'nin olmadığı yerlerde K içeren bitkisel küller kullanılıyordu.2O, yağlarla reaksiyona girmek ve sözde üretmek "gri sabun".
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/oxidos-basicos.htm

