Ö denklem dengeleme kimyasal denklemde bulunan atom sayısını eşleştirmemize izin verir, böylece gerçek olur ve bir kimyasal reaksiyonu temsil eder.
Bilginizi test etmek için aşağıdaki soruları kullanın ve sorularınızı cevaplamak için geri bildirimden sonra yorumlanan cevapları kontrol edin.
soru 1
(Mackenzie-SP)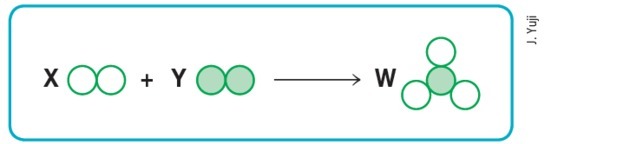
Boş ve dolu dairelerin sırasıyla farklı atomları ifade ettiğini varsayarsak, şema X, Y ve W harflerini sırasıyla şu şekilde değiştirirsek, yukarıdaki dengeli bir kimyasal reaksiyonu temsil edecektir. değerler:
a) 1, 2 ve 3.
b) 1, 2 ve 2.
c) 2, 1 ve 3.
d) 3, 1 ve 2.
e) 3, 2 ve 2.
Alternatif d) 3, 1 ve 2.
1. adım: Denklemin anlaşılmasını kolaylaştırmak için harfler atarız.
2. adım: denklemde en çok atomun kimde olduğunu bulmak için indeksleri toplarız.
| bu | |
| B |
A ve B, denklemin her bir üyesinde yalnızca bir kez görünür. Ancak indeksleri toplarsak A'nın en yüksek değere sahip olduğunu görürüz. Bu nedenle, onun için dengelemeye başladık.
3. adım: A öğesini, endeksleri yer değiştirerek ve katsayılara dönüştürerek dengeleriz.
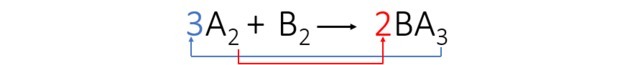
B elemanının otomatik olarak dengelendiğini ve denklemin katsayılarının 3, 1 ve 2 olduğunu gözlemledik.
soru 2
(Unicamp-SP) Aşağıdaki cümleyi okuyun ve semboller ve formüller kullanarak (dengeli) bir kimyasal denkleme dönüştürün: Molekül başına nitrojen, üç molekül diatomik, gaz halindeki hidrojen ile reaksiyona girerek, üç hidrojen atomundan ve bir tanesinden oluşan iki molekül gaz halinde amonyak üretir. azot".
Cevap:
Soruda açıklanan atomları temsil ederek, reaksiyonun aşağıdaki gibi gerçekleştiğini anlayabiliriz:
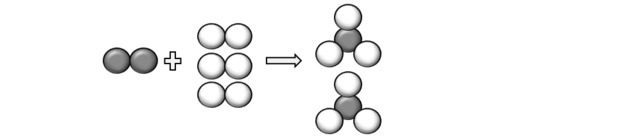
Böylece denkleme geliyoruz:
Soru 3
Hidrojen peroksit, aşağıdaki kimyasal denkleme göre ayrışabilen, su ve oksijen oluşturan kimyasal bir bileşiktir.
Bu reaksiyonla ilgili olarak, doğru dengelenmiş denklem şudur:
a) H2Ö2 →2 + H2Ö
b) 2 saat2Ö2 →2 + 2H2Ö
c) H2Ö2 → 2O2 + H2Ö
d) 2 saat2Ö2 → 2O2 + 2H2Ö
Doğru alternatif: b) 2H2Ö2 →2 + 2H2Ö
Hidrojen peroksitin iki kimyasal elementin atomlarından oluşan bir kimyasal olduğuna dikkat edin: hidrojen ve oksijen.
Ayrışma reaksiyonundan sonra, hem reaktanlarda hem de ürünlerde iki elementin aynı sayıda atomuna sahip olmalısınız. Bunun için denklemi dengelememiz gerekiyor.
Reaktanda 2 hidrojen atomumuz olduğuna dikkat edin (H2Ö2) ve üründeki iki atom (H2Ö). Bununla birlikte, oksijenin reaktanda iki atomu vardır (H2Ö2) ve ürünlerdeki üç atom (H2O ve O2).
2 katsayısını hidrojen peroksitin önüne koyarsak, elementlerin atom sayısını ikiye katlarız.
Su formülüyle aynı katsayıyı bir araya getirirsek, her iki tarafta da aynı miktarda atoma sahip olduğumuza dikkat edin.
Bu nedenle, doğru dengelenmiş kimyasal denklem 2H'dir.2Ö2 →2 + 2H2Ö.
4. soru
(UFPE) Aşağıdaki kimyasal reaksiyonları düşünün.
Şunu söyleyebiliriz:
a) hepsi dengelidir.
b) 2, 3 ve 4 denktir.
c) sadece 2 ve 4 dengelidir.
d) sadece 1 tanesi dengesizdir.
e) Tepkimeye girenlerin ve ürünlerin fiziksel durumları farklı olduğundan hiçbiri doğru şekilde dengelenmemiştir.
Alternatif b) 2, 3 ve 4 dengelidir.
Alternatif 1 ve 5 yanlış çünkü:
- Denklem 1 dengesizdir, doğru denge şöyle olacaktır:
- Denklem 5 yanlıştır çünkü reaksiyonda oluşan bileşik H olacaktır.2SADECE3.
H'yi oluşturmak için2SADECE4 SO oksidasyonu denklemine dahil edilmelidir2.
soru 5
(Mackenzie-SP) 800 °C'ye ısıtıldığında kalsiyum karbonat, kalsiyum oksit (saf kireç) ve karbondioksite ayrışır. Açıklanan fenomene karşılık gelen doğru şekilde dengelenmiş denklem şudur:
(Verilen: Ca - alkali toprak metali.)
alternatif c)
Kalsiyum bir alkali toprak metalidir ve kararlılığa sahip olması için kalsiyumun 2 elektrona ihtiyacı vardır (Ca2+), oksijen yükü olan (O2-).
Böylece, bir kalsiyum atomu bir oksijen atomuna bağlanır ve oluşan bileşik, sönmemiş kireç olan CaO'dur.
Diğer ürün karbondioksittir (CO2). Her ikisi de kalsiyum karbonattan (CaCO3).
Bir denkleme koymak:
Atom miktarlarının zaten doğru olduğunu ve dengelemeye ihtiyaç duymadığını not ediyoruz.
6. soru
(UFMG) Denklem dengeli değildir. Mümkün olan en küçük sayılarla dengelendiğinde, stokiyometrik katsayıların toplamı şöyle olacaktır:
a) 4
b) 7
c) 10
d) 11
e) 12
Alternatif e) 12
Deneme yöntemini kullanarak, dengeleme sırası şöyle olacaktır:
1. adım: Her üyede sadece bir kez görünen ve indeksi en yüksek element kalsiyum olduğu için dengelemeye başladık.
2. adım: Dengelemeyi radikal PO ile takip ediyoruz43-, bu da yalnızca bir kez görünür.
3. adım: hidrojeni dengeleriz.
Bununla oksijen miktarının otomatik olarak ayarlandığını ve denklemin dengesinin şu şekilde olduğunu gözlemliyoruz:
Katsayı 1 olduğunda, denkleme yazmanıza gerek olmadığını hatırlayarak.
Sahip olduğumuz katsayıları ekleyerek:
7. soru
Yanma, enerjinin ısı şeklinde salındığı bir kimyasal reaksiyon türüdür.
Karbon ve hidrojenden oluşan bir maddenin tamamen yanması sonucu karbondioksit ve su oluşur.
Hidrokarbon yanma reaksiyonlarını gözlemleyin ve aşağıdaki denklemlerden hangisinin yanlış dengelendiğini cevaplayın:
a) CH4 + 2O2 → CO2 + 2H2Ö
M.Ö3H8 +502 → 3CO2 + 4H2Ö
c)4H10 +13/3O2 → 4CO2 + 5s2Ö
d)2H6 + 7/2O2 → 2CO2 + 3H2Ö
Yanlış cevap: c) C4H10 +13/3O2 → 4CO2 + 5s2Ö
Kimyasal denklemleri dengelemek için önce denklemin her bir üyesinde hangi elementin yalnızca bir kez göründüğüne bakalım.
Karbon ve hidrojenin, sunulan her denklemde yalnızca bir reaktan ve bir ürün oluşturduğuna dikkat edin.
Öyleyse, daha fazla sayıda atoma sahip olduğu için hidrojenle dengelemeye başlayalım.
Bu nedenle, dengeleme sırası şöyle olacaktır:
- Hidrojen
- Karbon
- Oksijen
Hidrojen
Ürün 2 hidrojen atomuna sahip olduğundan, reaktandaki hidrojen atomlarının sayısıyla sonuçlanan 2 ile çarpılan bir katsayı olarak bir sayı ekleriz.
a) CH4 + O2 → CO2 + 2H2Ö
M.Ö3H8 + O2 → CO2 + 4H2Ö
c)4H10 + O2 → CO2 + 5H2Ö
d)2H6 + O2 → CO2 + 3H2Ö
Karbon
Dengeleme, reaktandaki karbon indeksinin yer değiştirmesi ve bu elementin atomlarına sahip ürün üzerinde bir katsayı olarak kullanılmasıyla yapılır.
a) CH4 + O2 → 1CO2 + 2H2Ö
M.Ö3H8 + O2 → 3CO2 + 4H2Ö
c)4H10 + O2 → 4CO2 + 5s2Ö
d)2H6 + O2 → 2CO2 + 3H2Ö
Oksijen
Oluşan ürünlerdeki oksijen atomlarının sayısını ekleyerek, reaksiyona girmesi gereken elementin atom sayısını buluruz.
Bunun için, ürünlerdeki oksijen atomlarının sayısını veren 2 ile çarpılan bir sayıyı katsayı olarak koymalıyız.
a) CH4 + O2 → 1CO2 + 2H2Ö
2x = 2 + 2
2x = 4
x = 2
Yani doğru denklem: CH4 + 2Ö2 → 1CO2 + 2H2Ö.
M.Ö3H8 + O2 → 3CO2 + 4H2Ö
2x = 6 + 4
2x = 10
x = 5
Yani doğru denklem: C3H8 + 5Ö2 → 3CO2 + 4H2Ö
c)4H10 + O2 → 4CO2 + 5s2Ö
2x = 8 + 5
2x = 13
x = 13/2
Yani doğru denklem: C4H10 + 13/2Ö2 → 4CO2+ 5s2Ö
d)2H6 + O2 → 2CO2 + 3H2Ö
2x = 4 + 3
2x = 7
x = 7/2
Yani doğru denklem: C2H6 + 7/2Ö2 → 2CO2 + 3H2Ö
Doğru dengelenmiş denklemler:
a) CH4 + 2O2 → CO2 + 2H2Ö
M.Ö3H8 +502 → 3CO2 + 4H2Ö
c)4H10 + 13/2O2 → 4CO2 + 5s2Ö
d)2H6 + 7/2O2 → 2CO2 + 3H2Ö
Böylece, alternatif c) C4H10 +13/3O2 → 4CO2 + 5s2Bunun nedeni, doğru dengeye sahip olmamasıdır.
soru 8
(Enem 2015) Kireçtaşları, kükürt dioksit (SO2) için sorbent görevi görebilen kalsiyum karbonattan oluşan malzemelerdir.2), önemli bir hava kirleticidir. Sürece dahil olan reaksiyonlar, kireçtaşının kalsinasyon yoluyla aktivasyonu ve SO2'nin sabitlenmesidir.2 basitleştirilmiş kimyasal denklemlerle gösterildiği gibi bir kalsiyum tuzu oluşumu ile.
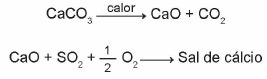
Bu kükürt giderme işleminde yer alan reaksiyonlar göz önüne alındığında, kalsiyum tuzunun kimyasal formülü şuna karşılık gelir:
alternatif b)
Reaksiyon dengelendiğinden, reaktanlarda bulunan atomların ürünlerde aynı miktarda olması gerekir. Böylece,
Oluşan tuz şunlardan oluşur:
1 kalsiyum atomu = Ca
1 kükürt atomu = S
4 oksijen atomu = O4
Bu nedenle, kalsiyum tuzunun kimyasal formülü CaSO'ya karşılık gelir.4.
9. soru
(UFPI) X'in Y ile reaksiyonu aşağıda gösterilmiştir. Hangi denklemin dengeli kimyasal denklemi en iyi temsil ettiğini belirleyin.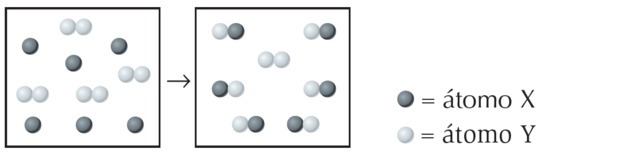
alternatif a)
Şekilde X türünün tek atom, Y türünün ise iki atomlu olduğunu yani 2 atomun birleşmesiyle oluştuğunu görüyoruz. Yani X, Y ile reaksiyona girer2.
Oluşan ürün XY ile temsil edilir, denklem dengesizdir:
Denklemi şu şekilde dengeleriz:
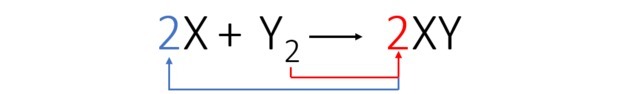
Dengeli denkleme göre, aşağıdaki şekil bize reaksiyonun nasıl oluştuğunu ve oranını göstermektedir.
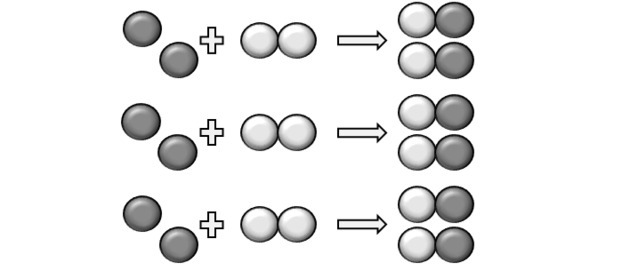
Bir reaksiyonun gerçekleşmesi için sabit bir oran olması gerekir ve bu nedenle bazı bileşikler reaksiyona girmeyebilir. Şekil bunu gösteriyor, çünkü üründe bir Y olduğunu görüyoruz.2 tepki vermedi.
10. soru
(Enem 2010) Gelecek nesiller için daha iyi bir gezegeni teşvik etme seferberlikleri giderek daha sık hale geliyor. Çoğu toplu taşıma aracı, şu anda bir fosil yakıt yakılarak çalıştırılmaktadır. Bu uygulamanın yol açtığı yüke örnek olarak, bir arabanın kat edilen km başına ortalama olarak yaklaşık 200 g karbondioksit ürettiğini bilmek yeterlidir.
Küresel Isınma Dergisi. Yıl 2, 8. Instituto Brasileiro de Cultura Ltda'nın Yayını.
Benzinin ana bileşenlerinden biri oktandır (C8H18). Oktan enerjisinin yanması sayesinde otomobilin hareket etmeye başlaması mümkündür. Bu işlemin kimyasal reaksiyonunu temsil eden denklem şunu gösterir:
a) işlem sırasında oksijen O şeklinde salınır.2.
b) su için stokiyometrik katsayı 8 ila 1 oktandır.
c) Süreçte su tüketimi vardır, böylece enerji açığa çıkar.
d) oksijenin stokiyometrik katsayısı 12,5 ila 1 oktandır.
e) karbon dioksit için stokiyometrik katsayı 9 ila 1 oktandır
Alternatif d) oksijen için stokiyometrik katsayı 12,5 ila 1 oktandır.
Denklemi dengelerken aşağıdaki katsayıları buluruz:
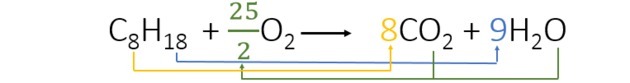
- Dengelemeye, her üyede sadece bir kez görünen ve daha yüksek bir indekse sahip olan hidrojen ile başladık. 18 reaksiyona giren hidrojen atomu olduğundan, üründe 2 tane vardır, bu yüzden 2 ile çarpı 18 veren bir sayı eklememiz gerekiyor. Yani 9 katsayıdır.
- Sonra CO'nun önüne 8 katsayısını ekliyoruz.2 denklemin her bir üyesinde 8 karbona sahip olmak.
- Son olarak, sadece üründeki oksijen miktarını ekleyin ve 2 ile çarpılan değeri bize 25 oksijen atomu veren değeri bulun. Bu yüzden 25/2 veya 12.5'i seçtik.
Böylece 1 oktanın yanması için 12,5 oksijen tüketilir.
11. soru
(Fatec-SP) Gübrelerin önemli bir özelliği suda çözünürlükleridir. Bu nedenle gübre endüstrisi, suda çözünürlüğü çok düşük olan kalsiyum fosfatı, kalsiyum süperfosfat olan çok daha çözünür bir bileşiğe dönüştürür. Bu süreç şu denklemle temsil edilir:
burada x, y ve z değerleri sırasıyla:
a) 4, 2 ve 2.
b) 3, 6 ve 3.
c) 2, 2 ve 2.
d) 5, 2 ve 3.
e) 3, 2 ve 2.
Alternatif e) 3, 2 ve 2.
Cebirsel yöntemi kullanarak, her element için denklemler oluştururuz ve reaktandaki atom sayısını üründeki atom sayısıyla eşitleriz. Bu nedenle:
Dengeli denklem:
soru 12
Aşağıdaki denklemleri deneme yöntemini kullanarak dengeleyiniz.
Cevap:
Denklem hidrojen ve klor elementlerinden oluşur. Sadece ürünün önüne katsayı 2 ekleyerek elemanları dengeliyoruz.
Atomların miktarları zaten ayarlanmış olduğundan denklemin dengelenmesine gerek yoktu.
Fosforun reaktanlarda iki atomu vardır, bu nedenle bu elementi dengelemek için üründeki fosforik asit miktarını 2H'ye ayarlıyoruz.3TOZ4.
Bundan sonra, üründe hidrojenin 6 atomu olduğunu gözlemledik, bu elementin miktarını, içerdiği reaktanta 3 katsayısı ekleyerek dengeledik.
Önceki adımlarla oksijen miktarı düzeltildi.
Denkleme baktığımızda, ürünlerdeki hidrojen ve brom miktarlarının ne kadar iki katı olduğunu görüyoruz. reaktiflerde varsa, bu ikisini dengelemek için HBr'ye 2 katsayısı ekleriz. elementler.
Klorun ürünlerde 3 atomu ve reaktanlarda sadece 1 atomu vardır, bu nedenle HCl'den önce 3'lük bir katsayı koyarak dengeleriz.
Hidrojenin reaktanlarda 3 atomu ve ürünlerde 2 atomu vardı. Miktarları ayarlamak için H indeksini dönüştürüyoruz2 katsayı olarak, HCl'de zaten bulunan 3 ile çarparız ve 6HCl sonucunu elde ederiz.
Ürünlerdeki klor miktarını da 6 atomlu olacak şekilde ayarlıyoruz ve 2AlCl elde ediyoruz.3.
Alüminyumun ürünlerde 2 atomu vardı, reaktanlardaki miktarı 2Al olarak ayarladık.
Üründeki hidrojen miktarını 3H ile dengeliyoruz2 ve bu elementin 6 atom miktarını denklemin her terimine sığdırıyoruz.
Denklemde nitrat radikali (NO3-) üründe indeks 2'ye sahipse, indeksi 2AgNO için reaktandaki katsayıya dönüştürüyoruz3.
Ayarlanması gereken gümüş miktarı, artık reaktiflerde 2 atoma sahip olduğundan, üründe 2Ag var.
Reaktanlarda 4 hidrojen atomumuz var ve bu elementi dengelemek için HCl ürününe 2 katsayısı ekliyoruz.
Klor artık ürünlerde 4 atoma sahiptir, bu nedenle reaktifteki miktarı 2Cl'ye ayarlıyoruz.2.
Reaktanlarda 6 hidrojen atomumuz var ve bu elementi dengelemek için su miktarını 3H'ye ayarlıyoruz.2Ö.
Reaktanlarda 2 karbon atomumuz var ve bu elementi dengelemek için karbondioksit miktarını 2CO'ya ayarlıyoruz.2.
Oksijenin reaktanlarda 7 atoma sahip olması gerekir ve bu elementi dengelemek için moleküler oksijen miktarını 3O'ya ayarlıyoruz.2.
Denkleme bakıldığında, nitrat radikali (NO3-) üründe indeks 2'ye sahiptir. AgNO reaktifinde indeksi katsayı 2'ye dönüştürüyoruz3.
Reaktanlarda 2 gümüş atomumuz var ve bu elementi dengelemek için üründeki gümüş klorür miktarını 2AgCl'ye ayarlıyoruz.
Üründe 3 kalsiyum atomumuz var ve bu elementi dengelemek için reaktifteki kalsiyum nitrat miktarını 3Ca'ya (NO3)2.
Daha sonra 6 NO radikali ile kalırız3- reaktanlarda ve bu radikali dengelemek için ürünlerdeki nitrik asit miktarını 6HNO'ya ayarlıyoruz.3.
Artık ürünlerde 6 hidrojen atomumuz var ve bu elementi dengelemek için reaktifteki fosforik asit miktarını 2H'ye ayarlıyoruz.3TOZ4.
Kimyasal denklemlerle hesaplamalar hakkında daha fazla bilgiyi şu adreste bulabilirsiniz:
- Dengeleyici kimyasal denklemler
- stokiyometri
- stokiyometrik hesaplamalar
- stokiyometri egzersizleri
- Periyodik tablo egzersizleri

