Maddeler, tüm özellikleri iyi tanımlanmış, belirlenmiş ve pratik olarak sabit olan malzemelerdir.
Üç örneğe bakın:
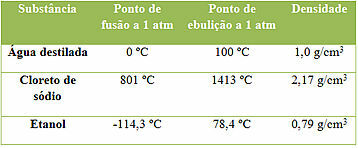
Üç maddeye örnekler ve özellikleri
Bunların üç madde olduğuna ve aynı sıcaklık ve basınç koşulları altında ölçüldüğünde özelliklerinin sabit olduğuna dikkat edin. Ancak hiçbir iki maddenin tüm özellikleri tam olarak aynı olmadığından, her birinin farklı özellik değerleri vardır. Bu önemlidir çünkü bir maddeyi tanımlamak için kullanılabilirler.
Atomlar maddenin en küçük bileşenleridir ve örneğin helyum (He) atomlarından oluşan helyum gazı durumunda olduğu gibi izole kalabilirler; fakat aynı zamanda çeşitli şekillerde de bağlanabilirler, moleküller oluştururlar (eşlerini paylaşarak kovalent olarak bağlananlar söz konusu olduğunda). elektronlar) veya iyonik kümeler (birinin diğerine kesin olarak elektron bağışladığı ve iyonların oluştuğu iyonik bağ ile bağlanan) çekmek).
Böylece, maddeler atomlar, moleküller veya iyonik kümeler tarafından oluşturulabilir. Su ve etanol, sırasıyla H olan moleküller tarafından oluşturulur.
2O ve C2H5OH, sodyum klorür ise üniter formülü NaCy olan iyonik aglomeralardan oluşur.
Su ve tuz maddelere örnektir
Bu örnekler, maddelerin kendilerini oluşturan atomların gruplarına göre sınıflandırılabileceğini göstermektedir. Maddeyi oluşturmak için birleşen atomlar aynı kimyasal elemente aitse, basit madde. Bazı örnekler şunlardır: oksijen gazı (O2), hidrojen gazı (H2), demir (Fe), helyum gazı (He), alüminyum (A?) vb.
Öte yandan, maddeler su, etanol ve sodyum klorür gibi iki veya daha fazla farklı elementin atomlarından oluşuyorsa, maddeler olarak sınıflandırılır. bileşik madde.
Doğada maddeleri izole, saf halde bulmak çok yaygın değildir. Genellikle diğer maddelerle karıştırılmış halde bulunurlar. Örneğin, içtiğimiz maden suyu sadece H molekülleri değil, birçok çözünmüş madde içerir.2Ö; bu yüzden o bir karıştır, ve madde değildir.
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-substancia.htm
