Kimyasal denge, Enem ve giriş sınavlarında en çok düşen konulardan biridir.
Sorularda tersinir reaksiyonların yönleri ele alınır ve adaylar hem hesaplamalarla hem de bu temayı içeren kavramlarla değerlendirilir.
Bunu akılda tutarak, kimyasal dengeye farklı yaklaşımlarla bu soru listesini hazırladık.
Sınavlara hazırlanmak için çözüm yorumlarından yararlanın ve soruların nasıl çözüleceğine ilişkin adım adım talimatlara göz atın.
Kimyasal dengenin genel kavramları
1. (Uema) Denklemde , kimyasal dengeye ulaştıktan sonra denge sabiti sonucuna varabiliriz
, bunun hakkında şunu söylemek doğru:
a) Kc değeri ne kadar yüksek olursa, doğrudan reaksiyon verimi o kadar düşük olur.
b) Kç sıcaklıktan bağımsız olarak.
c) İleri ve ters reaksiyonların hızları eşitse, Kc = 0 olur.
d) Kç reaktanların başlangıç molaritelerine bağlıdır.
e) Kc değeri ne kadar büyük olursa, ürünlerin konsantrasyonu o kadar büyük olur.
Doğru cevap: e) Kc değeri ne kadar büyükse, ürünlerin konsantrasyonu o kadar büyük olur.
Doğrudan reaksiyon, 1 sayısı ile temsil edilir, burada:
Ters reaksiyon ile temsil edilir
K'nin değeriç ürünlerin ve reaktiflerin konsantrasyonları arasındaki oran ile hesaplanır.
Pay (ürünleri içeren) denge sabiti ile doğru orantılıdır. Bu nedenle, K değeri ne kadar yüksek olursaç, daha fazla ürün oluştukça doğrudan reaksiyonun verimi ve sonuç olarak ürünlerin konsantrasyonu o kadar yüksek olur.
K'nin değeriç sıcaklığa göre değişir, çünkü değerini değiştirdiğimizde endotermik (ısı absorpsiyonu) veya ekzotermik (ısı salınımı) reaksiyonu olabilir. tercih edilir ve bununla daha fazla reaktif veya ürün tüketilebilir veya oluşturulabilir, böylece konsantrasyonuna bağlı olan denge sabiti değiştirilir. reaktifler.
Kc, denge kurulduğunda ve ileri ve geri reaksiyonların hızları eşit olduğunda bileşenlerin molar miktarlarına bağlıdır.
2. (UFRN) Kimyasal dengenin özelliği mikroskobik düzeyde dinamik olmasıdır. Kimyasal dengenin kapsamı hakkında nicel bilgi elde etmek için denge sabit miktarı kullanılır. Aşağıdaki şeridi göz önünde bulundurun:

Kimyasal dengeye uygulandığında, karakterin denge fikri:
a) Doğrudur çünkü kimyasal dengede miktarların yarısı her zaman ürün, diğer yarısı da reaktandır.
b) Kimyasal dengede ürünlerin ve tepkenlerin konsantrasyonları farklı olabileceğinden, ancak bunlar sabit olduğundan doğru değildir.
c) Doğrudur, çünkü kimyasal dengede, denge bir dış etki tarafından bozulmadığı sürece, reaktanların ve ürünlerin konsantrasyonları her zaman aynıdır.
d) Kimyasal dengede, denge bir dış faktörden etkilenmediği sürece ürünlerin konsantrasyonları her zaman reaktanların konsantrasyonlarından daha yüksek olduğu için doğru değildir.
e) Doğrudur çünkü kimyasal dengede tepkenlerin ve ürünlerin konsantrasyonları her zaman aynı değildir.
Doğru cevap: b) Kimyasal dengede ürünlerin ve tepkenlerin konsantrasyonları farklı olabileceğinden, ancak bunlar sabit olduğundan doğru değildir.
Dengede, ürün ve reaktiflerin miktarları aşağıdaki sabite göre hesaplanabilir. denge ve mutlaka ürün miktarının yarısı ve diğer yarısı olmamalıdır reaktifler.
Denge konsantrasyonları her zaman aynı değildir, farklı olabilir, ancak dengede herhangi bir bozulma olmazsa sabittir.
Denge konsantrasyonları, ister doğrudan ister ters olsun, hangi reaksiyonun tercih edildiğine bağlı olmalıdır. Bunu K değeri ile bilebiliriz.ç: eğer Kç 1, Doğrudan reaksiyon tercih edilir. zaten eğer Kç
1 ters reaksiyon tercih edilir.
Kimyasal Denge Tabloları
3. (UFPE) 20. yüzyılın başlarında Birinci Dünya Savaşı beklentisi azot bileşiklerine büyük bir ihtiyaç doğurmuştur. Haber, havadaki azottan amonyak üretimine öncülük etti. Amonyak kapalı bir kaba konulursa, aşağıdaki dengesiz kimyasal denkleme göre ayrışır: NH3(g) → H2(g) + H2(g). Konsantrasyonlardaki zaman içindeki değişimler aşağıdaki şekilde gösterilmektedir:

Yukarıdaki şeklin analizinden, A, B ve C eğrilerinin sırasıyla aşağıdaki reaksiyon bileşenlerinin konsantrasyonlarının zamansal varyasyonunu temsil ettiğini söyleyebiliriz:
a) H2, Hayır2 ve NH3
b) NH3, H2 ve hayır2
c) NH3, Hayır2 ve H2
d) Hayır2, H2 ve NH3
e) H2, ABD3 ve hayır2
Doğru cevap: d) N2, H2 ve NH3.
1. adım: kimyasal denklemi dengeleyin.
2 NH3(g) → H2(g) + 3 H2(g)
Dengeli reaksiyon ile 2 mol amonyağın nitrojen ve hidrojene ayrışmasının gerekli olduğunu anladık. Ayrıca, reaksiyonda üretilen hidrojen miktarı, amonyağınkinden üç kat daha fazladır.
2. adım: grafik verilerini yorumlayın.
Amonyak ayrışıyorsa, grafikte konsantrasyonu maksimumdur ve C eğrisinde görüldüğü gibi azalır.
Ürünler oluşurken reaksiyonun başlangıcında konsantrasyonlar sıfırdır ve reaktan ürün haline geldikçe artar.
Üretilen hidrojen miktarı nitrojeninkinden üç kat daha fazla olduğundan, bu gazın eğrisi B'de belirtildiği gibi en büyüğüdür.
Oluşan diğer ürün, A eğrisinde görüldüğü gibi azottur.
4. (Cesgranrio) Denklemin temsil ettiği sistem dengedeydi. Denge durumu, G maddesinin eklenmesiyle aniden değişti. Sistem dengeyi yeniden sağlamak için tepki verir. Aşağıdaki çizelgelerden hangisi açıklanan süreç sırasında meydana gelen değişiklikleri en iyi şekilde temsil eder?
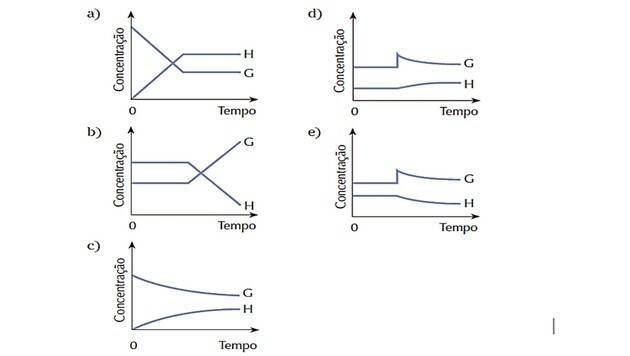
Doğru cevap: d).

Sistem başlangıçta dengede olduğu için G ve H maddelerinin miktarları sabit kalmıştır.
Bozulma, G konsantrasyonu arttıkça meydana geldi ve sistem bunu dönüştürerek tepki verdi. daha fazla H ürününde reaktan, dengeyi sağa kaydırır, yani reaksiyonu destekler doğrudan.
Reaktif eğrisi G'nin tüketildikçe azaldığını ve ürün eğrisi H'nin oluşurken arttığını gözlemliyoruz.
Yeni bir denge kurulduğunda, miktarlar tekrar sabit hale gelir.
Denge sabiti: konsantrasyon ve basınç arasındaki ilişki
5. (UFRN) K olduğunu bilmekP = Kç (RT)nk diyebilirizP = Kç, için:
çelik2(g) + H2(g) ↔ CO(g) + H2Ö(g)
b) H2(g) + ½2(g) ↔ H2Ö(1)
c) Hayır2(g) + 3 Saat2(g) ↔ 2 NH3(g)
d) HAYIR(g) + ½ O2(g) ↔ HAYIR2(g)
e) 4 FeS(ler) + 7 O2(g) ↔ 2 Fe2Ö3(ler) + 4 SO2(g)
Doğru cevap: a) CO2(g) + H2(g) ↔ CO(g) + H2Ö(g)
K'yeP K'ye eşit olmakç mol sayısındaki değişiklik sıfıra eşit olmalıdır, çünkü sıfıra yükseltilen herhangi bir sayı 1 ile sonuçlanır:
KP = Kç (RT)0
KP = Kç x 1
KP = Kç
Mol sayısındaki değişiklik şu şekilde hesaplanır:
∆n = Ürünlerin mol sayısı - Reaktiflerin mol sayısı
Bu hesaplamaya sadece gaz halindeki maddelerin katsayıları katılır.
Her alternatif denkleme uygulandığında, elimizde:
| çelik2(g) + H2(g) ↔ CO(g) + H2Ö(g) | ∆n = [(1+1) - (1+1)] = 2 - 2 = 0 |
| b) H2(g) + ½2(g) ↔ H2Ö(1) | ∆n = [0 - (1+1/2)] = 0 - 3/2 = - 3/2 |
| c) Hayır2(g) + 3 Saat2(g) ↔ 2 NH3(g) | ∆n = [2 - (1+3)] = 2 - 4 = - 2 |
| d) HAYIR(g) + ½2(g) ↔ HAYIR2(g) | ∆n = [1 - (1+1/2)] = 1 - 3/2 = - 1/2 |
| e) 4 FeS(ler) + 7 O2(g) ↔ 2 Fe2Ö3(ler) + 4 SO2(g) | ∆n = [(0+4) - (0+7)] = 4 - 7 = - 3 |
Bu sonuçlarla, değeri istenen sonuca karşılık gelen alternatifin birinci denkleminki olduğunu görebiliriz.
6. (UEL-uyarlanmış) ile temsil edilen reaksiyon için denge sabitleri Kç ve KP denklemlerle ifade edilir: (Verilen: p = kısmi basınç)
Doğru alternatif:
Denge sabiti şu şekilde hesaplanır:
Katı bileşikler, sabit konsantrasyonları nedeniyle K hesaplamasına katılmazlar.ç, bu nedenle, verilen denklem için denge sabiti:
Denge sabiti için, basınç cinsinden, hesaplamaya yalnızca gazlar katılır, bu nedenle:
Denge sabitinin hesaplanması
7. (Enem/2015) Atıklarını nehirler ve göller gibi su kütlelerinde bertaraf eden ve çevresel dengeyi etkileyebilecek endüstrilerde çeşitli asitler kullanılmaktadır. Asitliği nötralize etmek için, suyu nötralize eden bikarbonat ürettiği için atık suya uygun miktarlarda kalsiyum karbonat tuzu eklenebilir. Sürece dahil olan denklemler sunulur:
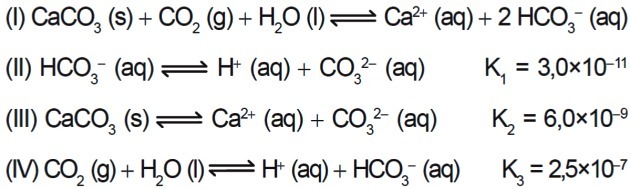
25°C'de II, III ve IV reaksiyonlarının denge sabitlerinin değerlerine dayanarak, reaksiyon I'in denge sabitinin sayısal değeri nedir?
a) 4,5 x 10-26
b) 5.0x10-5
c) 0.8 x 10-9
d) 0,2 x 105
e) 2,2 x 1026
Doğru cevap: b) 5.0 x 10-5
1. adım: Gerekli ayarlamaları yapmak için Hess yasasını kullanın.
Kimyasal bir denklem verildiğinde:
Sabit şu şekilde hesaplanır:
Ancak denklemi tersine çevirirsek, sonuç olarak şunu elde ederiz:
Ve sabit, tersi olur:
Soruda verilen denklem 1'e ulaşmak için önceki örnekte olduğu gibi denklem II'yi tersine çevirmemiz gerekiyor.
2. adım: I denkleminin sonucuna ulaşmak için II, III ve IV denklemlerini değiştirin.
3. adım: denklem I'in denge sabitini hesaplayın.
K hesaplamaben sabit değerler çarpılarak yapılır.
Hesaplamada tabanların kuvvetleri eşit olduğu için tabanı tekrar edip üsleri toplarız.
Artık tabanların kuvvetleri eşit olan bir bölmeye sahip olduğumuz için, tabanı tekrar edip üsleri çıkarıyoruz.
8. (UnB) Fosfor pentaklorür organik kimyada çok önemli bir reaktiftir. Reaksiyon yoluyla gaz fazında hazırlanır:
3.00 L kapasiteli bir şişe dengede, 200 °C'de: 0.120 mol PCl içerir5(g), 0.600 mol PCl3(g) ve 0.0120 mol CL2(g). Bu sıcaklıkta denge sabitinin değeri nedir?
Doğru cevap: 50 (mol/L)-1
1. adım: Reaksiyon için denge sabitinin ifadesini toplayın.
2. adım: dengede her bileşenin mol/L cinsinden konsantrasyonlarını hesaplayın.
Molar Konsantrasyon Formülü:
| PCl3 | Cl2 | PCl5 |
3. adım: sabit ifadedeki konsantrasyonları değiştirin ve K değerini hesaplayınç.
Denge dengesi uygulamaları
9. (Enem/2016) Lastikler tamamen aşındıktan sonra yakılarak enerji üretilebilir. Vulkanize kauçuğun tam yanması sonucu oluşan gazların bir kısmı kirleticidir ve asit yağmuruna neden olur. Atmosfere kaçmalarını önlemek için bu gazlar, uygun bir madde içeren sulu bir çözeltiye kabarcıklandırılabilir. Tabloda listelenen madde bilgilerini göz önünde bulundurun.
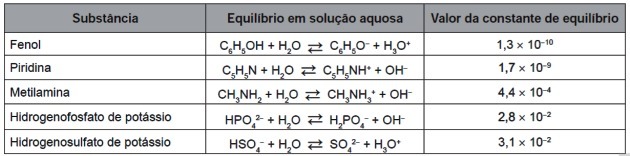
Tabloda listelenen maddelerden kirletici gazları en verimli şekilde uzaklaştırabileni (a)'dır.
a) Fenol.
b) Piridin.
c) Metilamin.
d) Potasyum hidrojen fosfat.
e) Potasyum hidrojen sülfat.
Doğru cevap: d) Potasyum hidrojen fosfat.
CO2, kükürt oksitler (SO2 ve bu yüzden3) ve azot oksitler (NO ve NO2) başlıca kirletici gazlardır.
Atmosferde bulunan su ile reaksiyona girdiklerinde, asit oluşumu yağmurun asitliğinin artmasına neden olur, bu yüzden asit yağmuru olarak adlandırılır.
Tabloda verilen denge sabitleri, ürünlerin ve reaktiflerin konsantrasyonları arasındaki oran ile aşağıdaki gibi hesaplanır:
Denge sabitinin ürünlerin konsantrasyonuyla orantılı olduğuna dikkat edin: Ürünlerin miktarı ne kadar büyükse, K değeri de o kadar büyük olur.ç.
K tablosundaki ilk ve son kompozitin değerlerini not edin.ç:
| piridin | ||
| potasyum hidrojen sülfat |
İki sayıyı karşılaştırdığımızda, negatif güç ne kadar küçükse, sabitin değerinin o kadar büyük olduğunu görüyoruz.
Kirleticileri daha verimli bir şekilde uzaklaştırmak için, OH- H iyonları ile reaksiyona girmek+ yoluyla asitlerde bulunur Nötrleştirme reaksiyonu.
Sunulan maddeler arasında asidik bileşikleri nötralize etmek için gerekli hidroksilleri üretenler şunlardır: piridin, metilamin ve potasyum hidrojen fosfat.
Hangi bileşiğin en verimli olduğunu bulmak için denge sabitlerini gözlemleriz: sabit değer ne kadar yüksek olursa, OH konsantrasyonu o kadar büyük olur.-.
Dolayısıyla, bu amaca uygun bir madde içeren sulu çözelti, daha bazik olduğundan ve asitleri daha verimli bir şekilde nötralize ettiğinden potasyum hidrojen fosfattır.
Daha fazla bilgi edinmek için bu metinleri okuyun.:
- iyon dengesi
- Nötrleştirme reaksiyonu
10. (Enem/2009) Sabunlar, uzun zincirli karboksilik asitlerin, yıkama işlemleri sırasında, suda çözünürlüğü düşük olan maddelerin, örneğin yağlar ve yağlar. Aşağıdaki şekil bir sabun molekülünün yapısını temsil etmektedir.
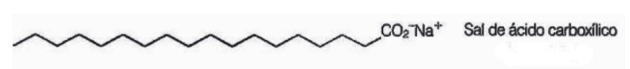
Çözeltide sabun anyonları suyu hidrolize edebilir ve böylece karşılık gelen karboksilik asidi oluşturabilir. Örneğin, sodyum stearat için aşağıdaki denge kurulur:
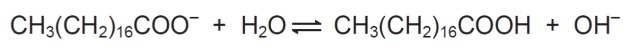
Oluşan karboksilik asit suda az çözünür ve yağların uzaklaştırılmasında daha az etkili olduğundan, Yukarıdaki dengenin sağa kaymasını önlemek için ortamın pH'ı kontrol edilmelidir.
Metindeki bilgilere dayanarak sabunların şu şekilde çalıştığı sonucuna varmak doğrudur:
a) Bazik pH'da daha verimlidir.
b) Asidik pH'da daha verimlidir.
c) Nötr pH'da daha verimli.
d) Herhangi bir pH aralığında verimli.
e) Asidik veya nötr pH'da daha verimlidir.
Cevap: a) Bazik pH'da daha verimli.
Gösterilen dengede, su ile reaksiyona girdiğinde sodyum stearatın bir karboksilik asit ve hidroksil oluşturduğunu görüyoruz.
pH'ı kontrol etmenin amacı karboksilik asit oluşumuna izin vermemektir ve bu, OH konsantrasyonu değiştirilerek dengeyi değiştirerek yapılır.-.
daha fazla OH- çözeltide, ürünler tarafında bir bozulma olur ve kimyasal sistem, konsantrasyonu artan maddeyi, bu durumda hidroksili tüketerek reaksiyona girer.
Sonuç olarak, ürünlerin reaktiflere dönüşümü olacaktır.
Bu nedenle, fazla hidroksil dengeyi sola kaydırdığı için sabunlar temel pH'da en verimli şekilde çalışır.
pH asidik olsaydı, daha yüksek bir H konsantrasyonu olurdu+ OH tüketerek dengeyi etkileyecek- ve denge, daha fazla hidroksil üreterek, dengeyi sola kaydırarak ve daha fazla karboksilik asit üreterek, sunulan işlemle ilgilenmeyecek şekilde hareket edecektir.
Kimyasal denge kayması
11. (Enem/2011) Alkolsüz içecekler giderek artan bir şekilde halk sağlığı politikalarının hedefi haline geldi. Tutkal ürünleri, diş matrisinin ana bileşeni olan mineral olan kalsiyumun sabitlenmesine zararlı bir madde olan fosforik asit içerir. Çürük, diş demineralizasyon sürecindeki dinamik bir dengesizlik, asitliğe bağlı mineral kaybı sürecidir. Diş minesinin ana bileşeninin hidroksiapatit adı verilen bir tuz olduğu bilinmektedir. Soda, sakarozun varlığı nedeniyle biyofilmin (bakteriyel plak) pH'ını düşürür ve diş minesinin demineralizasyonuna neden olur. Tükürük savunma mekanizmalarının pH seviyesini normalleştirmesi 20 ila 30 dakika sürer, bu da dişi yeniden mineralize eder. Aşağıdaki kimyasal denklem bu süreci temsil eder:
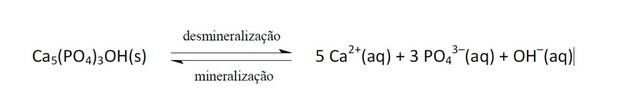 GROİSMAN, S. Sodanın dişler üzerindeki etkisi, diyetten çıkarılmadan değerlendirilir. Uygun: http://www.isaude.net. Erişim tarihi: 1 Mayıs 2010 (uyarlandı).
GROİSMAN, S. Sodanın dişler üzerindeki etkisi, diyetten çıkarılmadan değerlendirilir. Uygun: http://www.isaude.net. Erişim tarihi: 1 Mayıs 2010 (uyarlandı).
Bir kişinin günlük olarak alkolsüz içecekler tükettiği düşünüldüğünde, artan konsantrasyon nedeniyle diş demineralizasyon süreci meydana gelebilir.
a) OH–Ca iyonları ile reaksiyona giren2+, denge sağa kaydırılıyor.
b) H+OH hidroksilleri ile reaksiyona giren–, denge sağa kaydırılıyor.
c) OH–Ca iyonları ile reaksiyona giren2+, denge sola kaydırılıyor.
d) H+OH hidroksilleri ile reaksiyona giren–, denge sola kaydırılıyor.
e)2+OH hidroksilleri ile reaksiyona giren–, denge sola kaydırılıyor.
Doğru cevap: b) H+OH hidroksilleri ile reaksiyona giren–, denge sağa kaydırılıyor.
pH düştüğünde bunun nedeni asitliğin, yani H iyonlarının konsantrasyonunun artmasıdır.+, açıklamada belirtildiği gibi, fosforik asit varlığı var.
Bu iyonlar OH ile reaksiyona girer.- sistem bu uzaklaştırılan iyonlardan daha fazlasını üreterek hareket ettiğinden, bu maddenin tüketilmesine ve dolayısıyla dengenin sağa kaymasına neden olur.
OH konsantrasyonundaki azalma nedeniyle reaktanlar ve ürünler arasındaki denge kayması meydana geldi.-.
Ca iyonları ise2+ ve oh- konsantrasyon artmış olsaydı, sistem onları tüketerek ve daha fazla hidroksiapatit oluşturarak reaksiyona gireceği için dengeyi sola kaydıracaktı.
Açıklanan koşullar altında soğutucu sızıntısı ile ilgili önceki dengenin değiştirilmesi:
a) CO salınımı2 Çevre için.
b) Kabın sıcaklığını yükseltmek.
c) Kabın iç basıncını yükseltmek.
d) CO konsantrasyonunun yükselmesi2 sıvı içinde.
e) Önemli miktarda H oluşumu2Ö.
Doğru cevap: a) CO salınımı2 Çevre için.
Şişenin içindeki karbondioksit, yüksek basınç nedeniyle sıvı içinde çözüldü.
Şişe açıldığında, kabın içindeki basınç (ki daha büyüktü) ortamdaki basınca eşittir ve bununla birlikte karbondioksit çıkışı olur.
Reaktanlar ve ürünler arasındaki denge kayması, basınçtaki azalma nedeniyle meydana geldi: basınç düştüğünde, denge en büyük hacme (mol sayısı) kayar.
Reaksiyon sola kaymış ve CO2 Sıvı içinde çözülen, şişe açıldığında dışarı sızarak serbest bırakıldı.

