Süblimleşme, sıvı halden geçmeden katı halden gaz hale veya tam tersine geçiştir.
Bir maddenin süblimleşme işlemine tabi tutulabilmesi için belirli sıcaklık ve basınç değerlerine tabi tutulması gerekir.
Mothballs ve CO2 katı (kuru buz), ortam koşulları altında süblimleşmeye uğrayan maddelere örnektir.

fazlar diyagramı
Bir maddenin maruz kaldığı sıcaklık ve basınç değerlerini bilerek fiziksel durumunu keşfedebiliriz.
Bunun için deneysel olarak bulunan değerlerden her madde için oluşturulmuş diyagramları kullanıyoruz.
Aranan "fazlar diyagramı" katı, sıvı ve gaz hallerini temsil eden üç bölgeye ayrılmıştır. Bu bölgeleri sınırlayan çizgiler, maddenin faz değiştirdiği noktaları işaret eder.
Diyagramdaki üçlü nokta, maddenin üç fazda bir arada bulunabileceği sıcaklık ve basıncı gösterir. Bu noktanın altında süblimasyon eğrisi bulunur.
Bu eğri üzerindeki noktalar, süblimleşmenin gerçekleşeceği basınç ve sıcaklık değerlerini belirler.
Bir katı, üçlü noktadan daha düşük bir basınca maruz kaldığında, ısıtılırsa doğrudan gaz haline geçer.
Doğrudan katı halden gaz haline geçiş, sıcaklığı üçlü noktadan daha düşük olduğunda basıncın düşürülmesiyle de gerçekleşebilir.
Daha fazla bilgi edinin: Fiziksel Durum Değişiklikleri.
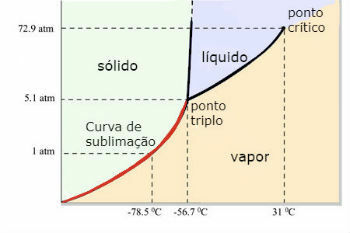
Karbon Dioksit (CO) Faz Diyagramı2 )
CO üçlü noktası2 basınç 5 atm olduğunda oluşur. Bu gerçek, ortam basıncı 1 atmosfer olduğu için kuru buzda süblimleşmenin görülmesinin yaygın olduğunu haklı çıkarır.
Bu nedenle ortam koşullarında sıvı karbon dioksit elde edilmez. Bu koşullar altında ya katı haldedir ya da buhar halindedir.
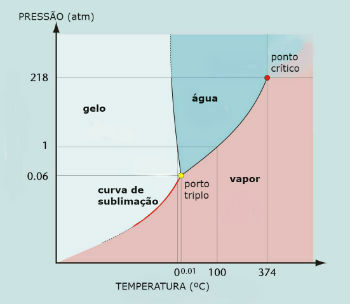
Su faz diyagramı (H2Ö)
Suyun üçlü noktası, basınç sadece 0,06 atm olduğunda meydana gelir. Bu nedenle, ortam koşulları altında suyun süblimleşmesi yaygın değildir.
Daha fazlasını öğrenmek için şunu da okuyun:
- Suyun Fiziksel Halleri
- Maddenin Fiziksel Halleri
- Sıvılaşma veya Yoğunlaşma
- Madde Özellikleri
- Katılaşma
- Füzyon
- buharlaşma
- Kaynamak
- buharlaşma