Klor, Cl sembolü, atom numarası 17, atom kütlesi 35.5 olan kimyasal bir elementtir. Halojen ailesine, grup 17 veya 7A'ya ve periyodik tablonun üçüncü periyoduna aittir.
Adı Yunancadan geliyor khloros, yeşilimsi anlamına gelir. Bunun nedeni, normal sıcaklık ve basınç koşulları altında, klorun güçlü bir kokuya sahip yeşilimsi sarı bir gaz olarak nitelendirilmesidir.
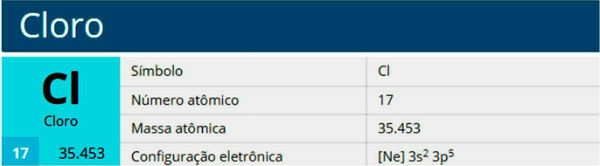
Özellikleri
Klor, 1774 yılında İsveçli bilim adamı Carl Wilhelm Scheele (1742-1786) tarafından keşfedildi. Ancak o zamanlar oksijenli bir bileşik olduğuna inanıyordum. 1810'da Humphry Davy (1778-1829) bunun yeni bir kimyasal element olduğunu gösterdi.
Son derece reaktif bir element olduğu için, volkanik patlamalar sırasında açığa çıkan HCl formundaki küçük bir miktar dışında saf haliyle doğada pek bulunmaz.
Bu nedenle, genellikle sofra tuzu olarak da bilinen sodyum klorür (NaCl) formunda bulunur. Minerallerde karnalit ve silvit şeklinde oluşur.
Ayrıca şuradan da elde edilebilir: elektroliz sulu çözelti içinde NaCl. Klor ayrıca, proses yoluyla klorürlerden birçok tuz üretir. oksidasyon.
Daha fazla bilgi edinin, ayrıca okuyun:
- Periyodik tablo
- Kimyasal elementler
- halojenler
uygulamalar
Klor gazı (Cl2) zehirli ve tahriş edicidir, bu durum 1. Dünya Savaşı sırasında kimyasal silah olarak kullanılmasına neden olmuştur. Bu gaz solunum yollarında ve deride tahrişe, akciğerlerde su tutulmasına, yırtılmaya ve çok miktarda solunduğunda ölüme neden olabilir.
Klorun diğer bazı kullanımları şunlardır:
- Klor dioksit (ClO) kullanılarak kağıt ve kumaşların ağartılması2).
- Su arıtma, klor ilavesi suyu içilebilir ve insan tüketimine uygun hale getirir. Bu işleme klorlama denir ve hipokloröz asit (HClO) kullanır.
- Klor mikroorganizmaları öldürme yeteneğine sahip olduğundan, yüzme havuzu suyunun ve endüstriyel atıkların dezenfeksiyonu.
- PVC (polivinil klorür) ve sentetik kauçuk gibi plastik bileşiklerin üretimi.
- Bazı organik ve inorganik bileşiklerin üretimi.


