Sen oksitler biri oksijen olan ve ikisinin en elektronegatifi olması gereken iki farklı elementten oluşurlar.
İnorganik oksitlerin isimlendirilmesi, oksidin moleküler, kovalent veya iyonik olmasına bağlı olan kuralları takip eder. Her bir duruma bakalım:
* Moleküler oksitlerin veya kovalent ağların isimlendirilmesi:
Moleküler veya kovalent ağ oksitler, oksijene bağlı olanlardır. Metaldiğerleri arasında karbon (C), azot (N), kükürt (S), flor (F) gibi. Bu oksitlerin isimlendirilmesi aşağıdaki kuralı takip eder:

Ametallerle oluşturulan oksitler için isimlendirme kuralı
Oksijen bağlantılı elemanın önündeki mono önek isteğe bağlıdır.
Örneğin, aşağıdaki moleküler oksite sahibiz: CO.
- Oksijen miktarını gösteren ön ek: 1 oksijen: mono;
- oksit;
- Diğer elementin atom sayısını gösteren önek: 1 karbon: mono;
- Oksijene bağlı elementin adı: karbon.
Yani adınız şöyle: CO = monokarbon monoksit veya karbonmonoksit.
Daha fazla örneğe bakın:
karbondioksit - CO2
Kükürt trioksit - SO3
Dikloro Heptoksit - Cl2Ö7
Dinitrojen Monoksit - N
Dinitrojen trioksit - N2Ö3
Azot Monoksit -NO
Azot dioksit - HAYIR2
Dinitrojen pentoksit - N2Ö5
Silikon dioksit - SiO2
Difosfor pentoksit - P2Ö5
Kükürt trioksit - SO3
* İyonik oksitlerin isimlendirilmesi:
İyonik oksitler, oksijene bağlı olanlardır. metaldiğerleri arasında demir (Fe), kurşun (Pb), sodyum (Na), kalsiyum (Ca), gümüş (Ag) gibi. Genel olarak, oksijenin elektrik yükü -2'dir.
Moleküler veya kovalent ağ oksitler için belirtilen isimlendirme şu anda metalik oksitlere de uygulanmaktadır ve resmi olarak kabul edilmektedir.. Bazı örneklere bakın:
Demir Monoksit - FeO
Kurşun Monoksit - PbO
Kurşun Dioksit - PbO2
Farklı trioksit - Fe2Ö3
Bununla birlikte, hala yaygın olarak kullanılan metal oksitler için özel bir isimlendirme vardır. Oksijene bağlı elementin değerliliğine dayanır.
eleman varsa tek değerlik, yani oksijene bağlanmanın ve yalnızca bir tür oksit oluşturmanın tek bir yolu varsa, adlandırma kuralı şu şekilde verilecektir:

Tek değerli iyonik oksit adlandırma kuralı
Örnekler:
- Sodyum oksit - Na2Ö
- Kalsiyum Oksit - CaO
- Potasyum oksit - K2Ö
- Alüminyum Oksit - Al2Ö3
- Gümüş oksit - Ag2Ö
Ancak elementlerin oluşturduğu iyonik oksitler de vardır. birden fazla değerlik. Bu durumlarda, adlandırma kuralı aşağıdaki gibidir:
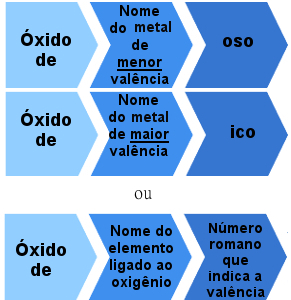
Birden fazla değerlikli iyonik oksitler için isimlendirme kuralı
Örnekler:
Demir Oksit - FeO
Demir Oksit - Fe2Ö3
Bakır Oksit - Cu2Ö
bakır oksit - CuO
Veya:
Demir oksit II - FeO (Demir nox = +2)
Demir oksit III - Fe2Ö3 (Demir nox = +3).
Bakır Oksit I - Cu2O (Demir nox = +1)
Bakır oksit II - CuO (Demir nox = +2).
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm