Karbon, atom numarası (Z) 6'ya eşit olan kimyasal bir elementtir; bu, onu oluşturan atomların çekirdeğinde altı proton olduğu anlamına gelir. Molar kütlesi 12.011 g/mol'dür ve doğada karbonun üç izotopu bulunur, bunlar: o karbon-12, karbon-13 ve karbon-14. C-12'nin çekirdeğinde altı proton ve altı nötron bulunur ve en bol olanıdır.
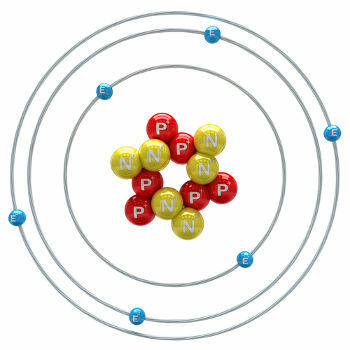
karbon-12 atomu illüstrasyonu
C-13'ün yedi nötronu vardır ve en az bol olanıdır (%1,01 ila %1,14). C-14'ün sekiz nötronu vardır ve bir radyoaktif element β parçacıkları (elektronlar) yayan, kozmik ışın nötronları atmosferin bu üst katmanlarında bulunan Azot-14'ü bombaladığında Dünya'nın stratosferinde oluşan. Tüm bitki ve hayvanlarda bulunur ve yarı ömrünün yaklaşık 5730 yıl olduğu bilindiğinden, fosillerin 100 ila 40.000 yıl arasındaki yaşını belirlemek için kullanılır. C-14 ve tarihleme tekniği hakkında daha fazla ayrıntı metinde görülebilir. Karbon-14 nedir?
Karbon dört değerlidir, yani oktet kuralına uymak için değerlik katmanında (en dış katman) dört protona daha ihtiyacı vardır. Bu nedenle, genellikle dört çift elektronu diğer elementler ve diğer karbonlarla paylaşan dört kovalent bağ yapar. Bu bağlar tekli, ikili veya üçlü olabilir ve milyonlarca farklı bileşiğin oluşmasına neden olur. Bu nedenle bir Kimya alanı oluşturulmuş,
Organik Kimyagibi mineral kökenli bazı durumlar dışında, karbondan türetilen ana bileşikleri inceleyen karbondioksit (CO2), Ö karbon monoksit (CO), Ö kalsiyum karbonat (CaCO3), sodyum hidrojen karbonat veya sodyum bikarbonat (NaHCO3), diğerleri arasında. Bu bileşikler incelenir İnorganik kimya.Karbon, basit maddeler, yani yalnızca karbon atomları arasındaki bağlardan oluşan maddeler oluşturan allotropi gerçekleştirir. Grafit (alfa ve beta), elmas, lonsdaleit (altıgen elmas), kaoit, karbon (VI) ve fullerenler olmak üzere en az yedi karbon allotropu vardır. Aslında, sentetik allotropik karbon formları olan birkaç çeşit fulleren vardır. Her tepe noktasında bir karbon atomu bulunan çokyüzlü bir yapıya sahiptirler ve bir örnek, Ç60 aranan buckminsterfullereneve yapısı bir futbol topuna benziyor.
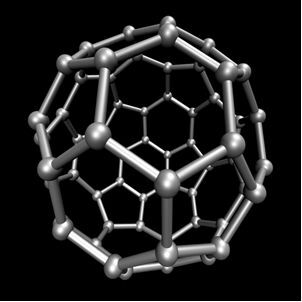
Karbon-60 (buckminsterfullerene)
Bununla birlikte, bu karbon allotropları arasında doğal olan sadece iki tane vardır. grafitşuradan Elmas. Aşağıdaki şekilde gösterildiği gibi, yalnızca atomların uzaydaki kristal dizilimi ile farklılık gösterirler ve bu, tamamen farklı fizikokimyasal özelliklerle sonuçlanır. Metni oku karbon allotropisi daha fazla bilgi için.

Karbonun iki doğal allotropik formu grafit ve elmastır.
Karbonun başka bir sentetik allotropik formu, nanotüpler (aşağıdaki resim) tıbbi teşhis ve tedaviler de dahil olmak üzere geniş biyolojik uygulamalara sahiptir.

Mikroskobik karbon nanotüp çizimi
Böylece, karbon çevremizdeki her şeyde ve içimizde mevcutturçünkü beste yapıyor doğal organik bileşikler — petrol, kömür ve doğal gaz içeren fosil yakıtlar ve etanol ve biyoyakıtlar gibi diğer yakıtlar - tarım ürünleri gibi. şekil de sentetik organik bileşiklerkumaşları oluşturan sentetik lifler, ilaçlar, plastikleri ve kauçukları oluşturan polimerler, böcek öldürücüler, boyalar ve çok daha fazlası gibi. İçimizde, hayvanlarda ve sebzelerde karbon, şeker, glikoz ve selüloz gibi karbonhidratlar gibi çok önemli bileşikler oluşturur; örneğin DNA'yı oluşturan proteinler ve lipitler ile birlikte kırmızı kan hücrelerinin ve beyaz kan hücrelerinin zarlarını oluştururlar.
Tüm bunlar, karbonun yaşamı sürdürmek için ne kadar önemli olduğunu gösteriyor. Ama aynı zamanda, şiddetin yoğunlaşması gibi olumsuz yönlerle de ilişkilendirilmiştir. sera etkisi ve bunun sonucu küresel ısınma, bunun nedeni, bu sorunların ana kötüsünün karbon dioksit bileşiği (CO2). Esas olarak bu gazı açığa çıkaran fosil yakıtların büyük oranda yanması nedeniyle CO konsantrasyonu2 atmosferde artmıştır. Sera gazı olarak yukarıda belirtilen sorunlara neden olur. Öte yandan, fotosentez ve solunum gibi hayati reaksiyonlarda da karbondioksit bulunur.
Jennifer Foğaça tarafından
Kimya mezunu
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-carbono.htm
