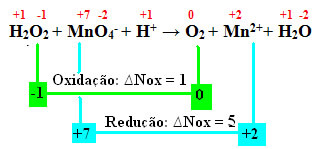
"Maddelerin polaritesi ve çözünürlüğü arasındaki ilişki" metninde, genellikle çözünenlerin polar maddeler, aynı zamanda polar olan çözücülerde çözünür ve polar olmayan maddeler de çözücülerde çözünür polar olmayan. Ancak bu, tüm çözünürlük durumları için geçerli olabilecek bir kural değildir.
Örneğin şeker suda erir, yağ ise erimez. Su ve şeker moleküllerinin polar, yağ moleküllerinin ise polar olmadığı doğrudur, ancak bunlar Bu izole maddelerin molekülleri ile birbirleri arasındaki moleküller arası kuvvetler bize bunun açıklamasını sağlar. gerçek.

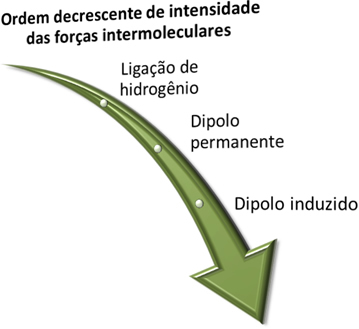
Bu kuvvetlerin ne olduğunu görmeden önce, bir yoğunluk meselesi olarak şunu hatırlayın: hidrojen bağı daha güçlüdürBunu kalıcı dipol kuvveti takip eder ve en zayıfı indüklenmiş dipol kuvvetidir.
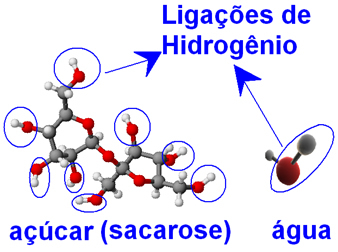
Hem su hem de şeker molekülleri (sakaroz - C12H22Ö11), hidrojen atomlarına bağlı oksijen atomları sunar, gruplar oluşturur ─ O ─ H. Bunun anlamı şudur ki su molekülleri arasında ve şeker molekülleri arasında moleküller arası hidrojen bağı etkileşimleri olabilir.
Bu nedenle su molekülleri, birbirine sıkıca bağlı olan şeker moleküllerini kristaller halinde sarabilir ve onları ayırarak yeniden birleşmelerini engelleyebilir. Böylece şekerin suda çözünürlüğü yüksektir ve 20ºC'de 100 g suda 33 g'a kadar çözebiliriz.
Artık yağ ve su karışmaz. Bu, yağın şekli değil, suyun yüzeyine yayıldığı için suyu çekmediği anlamına gelmez. küresel, bize daha fazla miktarda yağ molekülünün yağ molekülleri ile temas halinde olduğu bir şekil aradığını ortaya koyuyor. Su.
Şimdi durma... Reklamdan sonra devamı var ;)
Ancak, su molekülleri arasındaki çekim, yağ ve su molekülleri arasındaki çekimden çok daha fazladır (hidrojen bağı).. Bu nedenle, yağ molekülleri iki komşu su molekülü arasındaki bağı kıramaz.
Bu bizi şu sonuca götürür:
"Mevcut moleküller arası kuvvet olası yeni etkileşimden daha yoğunsa, o zaman çözünen çözünmez, orijinal bağ kalır. Ancak yeni etkileşim daha güçlüyse, çözünen maddenin moleküller arası bağlarını kırarak çözünecektir.”
Materyallerin çözünürlüğü için moleküller arası kuvvetlerin önemini bize gösteren bir başka örnek, iyot, su ve benzene sahip olduğumuz zamandır. Aşağıdaki şemada, iyotun benzende iyi çözündüğünü ve suda az çözünür olduğunu görüyoruz, su ve benzen tamamen karışmaz ve benzen ve su karışımımız olduğunda ve sonra iyot eklediğimizde, sadece içinde çözünür benzen:
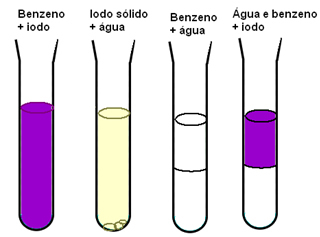
Benzen ve iyot polar değildir, polar olan sudan daha kolay karışma süresine sahiptir. Ancak gerçekte ne olduğunu açıklayan şey, polar olmayan moleküller arasında var olan moleküller arası uyarılmış dipol kuvvetlerinin suyun hidrojen bağlarına kıyasla zayıf olmasıdır.
Bu nedenle, su molekülleri arasındaki mevcut etkileşimler olası yeni etkileşimlerden daha güçlü olduğundan etkileşimler, hidrojen bağları kırılmaz ve benzen ile karıştırıldığında iki fazlı bir sistem gözlenir. Su.
İyot molekülleri ile benzen molekülleri arasında oluşan yeni etkileşimler, bu izole maddelerin molekülleri arasında oluşanlardan daha yoğundur.
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Maddelerin Moleküller Arası Dayanımı ve Çözünürlüğü Arasındaki İlişki"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/relacao-entre-forca-intermolecular-solubilidade-das-substancias.htm. 27 Haziran 2021'de erişildi.