Nitratlar, NO anyonunu içeren inorganik bileşiklerdir.3-.
Azot 15 ailesindendir, değerlik kabuğunda 5 elektrona sahiptir ve üç kovalent bağ yapması gerekir. (paylaşımlı elektronlarla) değerlik kabuğunda sekiz elektrona sahip olmak ve böylece kalmak kararlı. Bununla birlikte, her oksijenin son kabuğunda 6 elektronu vardır ve bu nedenle atomlarının her birinin kararlı olması için iki bağ yapması gerekir.
Nitrat anyonunda nitrojen, oksijenlerden biriyle çift bağ yapan merkezi elementtir. kararlı olan, diğer iki oksijenden biri ile tek bir bağ ve diğeri ile bir kovalent bağ datif. Bu, oksijenlerden birinin kararlı olmadığı, 1 elektron daha alması gerektiği ve -1'e eşit bir toplam yük verdiği anlamına gelir. Dative nitrojen ile yapabileceğinden daha fazla bağ kurar, elektronlarından birini bağışlayarak +1'e eşit bir yük alır. Bu anyonun yapısına bakın:
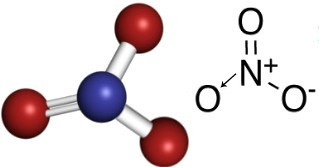
Bu anyon bir elektron alabilir ve elektriksel olarak nötr bir bileşik, bir inorganik tuz oluşturabilir. Bu bileşiklerin tümü suda çözünür.
Nitratların ana uygulamaları, anjina pektoris tedavisinde vazodilatörler gibi ilaçlardır. kalp kasına kan akışıyla düşük oksijen kaynağının neden olduğu) ve erektil disfonksiyon erkek. Daha sonra bahsedileceği gibi gübre ve patlayıcılarda da kullanılırlar.
Nitratlar, bir nitrik asit (HNO) nötralizasyon reaksiyonu yoluyla üretilebilir.3) bazı temel ile. Magnezyum nitratın oluştuğu aşağıdaki örneğe bakın:
HNO3 + Mg (OH)2 → Mg (HAYIR3)2+ H2Ö
Bu tür bileşiklerin üç ana örneği, sodyum nitrat (NaNO3), potasyum nitrat (KNO3) ve amonyum nitrat (NH4ŞEHİR3). Bütün bu durumlarda, katyonlar (Na+,K+ ve NH4+) bir nitrat anyonu için 1 elektron sağlar. Ancak gerçekte, bu zıt yükler birbirini çeker ve kristal kafesler olan iyi tanımlanmış iyonik kümeler oluşturur. Bu nedenle nitratlar, sodyum nitrat durumunda aşağıda gösterildiği gibi genellikle kristal katılardır:
Şimdi durma... Reklamdan sonra devamı var ;)
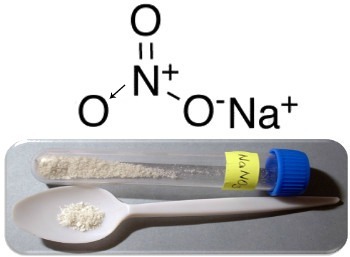
Bu bileşik gübre üretiminde kullanılır, ancak esas olarak şu şekilde bilinir: Şili güherçilesi, çünkü Şili çöllerinde büyük birikintileri var. Çeşitli silah ve patlayıcılarda kullanılan kara barutun yapımında kullanılan potasyum nitrata dönüştürülür.

Hem sodyum nitrat hem de potasyum nitrat, yaygın olarak kullanılan "güherçile" olarak adlandırılır. konserve ve tütsülenmiş etlerin renginin koruyucuları ve ayrıca bazı gıdalarda daha fazla lezzet hissi vermek için tokluk. Bununla birlikte, bu nitratlar bakteriler tarafından bakteri tarafından dönüştürülebildiğinden, bunların tüketimi sağlığa ciddi zararlar verir. organizmayı nitritlere ve daha sonra kanserojen olan nitrozaminlere dönüştürür ve esas olarak vücutta kansere neden olur. mide. Nitritler ayrıca kandaki hemoglobinleri dönüştürerek oksijen taşıyamazlar.
Nitratların fazla alınmasının başlıca nedenleri sebze yetiştiriciliğinde azotlu gübrelerin kullanılmasıdır.
Güherçile ayrıca tehlikelidir çünkü vücuttaki sodyum iyonlarının konsantrasyonunu arttırır, bu da yüksek tansiyon gibi kalp sorunlarına neden olabilir.
Ö amonyum nitrat aynı zamanda gübre ve patlayıcı olarak kullanılıyor ve hatta 11 Eylül 2001'de Dünya Ticaret Merkezi binalarına yapılan terörist saldırıda akaryakıtla birlikte kullanıldı.

Dünya Ticaret Merkezi'ne yapılan saldırıda amonyum nitrat kullanıldı*
* Görüntü telif hakkı: Dan Howell ve Shutterstock.com
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Nitratlar"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/nitratos.htm. 27 Haziran 2021'de erişildi.
Kimya

Günlük tuzlar, kalsiyum karbonat, sodyum klorür, sodyum florür, potasyum nitrat, sodyum nitrat sodyum, sodyum karbonat, sodyum bikarbonat, sodyum bikarbonat, sodyum sülfit, güherçile, soda.



