Özgül ısı, bir maddenin aldığı ısı miktarı ile onun termal değişimi arasında ilişki kuran fizik tarafından incelenen bir miktardır.
Olarak da adlandırılır termal kapasite, bu büyüklük, herhangi bir maddenin bir gramının bir değişime uğraması için gereken ısı miktarını gösterir. bir ısı kaynağına maruz kaldığında malzemenin davranışını belirtmeye ek olarak 1°C'ye karşılık gelen sıcaklık.
Özgül ısı doğrudan Fizik adı verilen alanla bağlantılıdır. kalorimetridaha yüksek sıcaklıktaki bir vücuttan daha düşük sıcaklıktaki başka bir vücuda enerji transferlerini inceleyen bilim dalı.
Bu çalışmada, özgül ısı, duyulur ısı ve ısıl kapasitenin tanımında yer almaktadır. Bir malzeme, çünkü bazı fenomenler ısı tanımından daha iyi anlaşılabilir. özel.
Ve özgül ısı ne kadar büyükse, termal değişime sahip olması için maddeden sağlanması veya çıkarılması gereken ısı miktarı da o kadar fazladır.
Örneğin su, diğer maddelerle karşılaştırıldığında, 1 cal/g.ºC'ye karşılık gelen en yüksek özgül ısıya sahiptir.
Spesifik ısı değerlerinin karşılaştırma tablosu
Diğer madde ve malzemelerin de aşağıdaki tabloda gösterildiği gibi kendi özgül ısı değerleri vardır:
| Madde | Özgül Isı (cal/g.ºC) |
| Su | 1 kal/g.°C |
| Etil alkol | 0,58 kal/g.°C |
| Alüminyum | 0,22 kal/g.°C |
| Hava | 0.24 kal/g.°C |
| Kum | 0,2 kal/g.°C |
| Karbon | 0.12 kal/g.°C |
| Öncülük etmek | 0.03 kal/g.°C |
| Bakır | 0.09 kal/g.°C |
| Demir | 0.11 kal/g.°C |
| buz | 0,50 kal/g.°C |
| Hidrojen | 3.4 kal/g.°C |
| Odun | 0,42 kal/g.°C |
| Azot | 0.25 kal/g.°C |
| Oksijen | 0,22 kal/g.°C |
| Bardak | 0.16 kal/g.°C |
Özgül ısı formülü
Maddelerin özgül ısısını bilmek için aşağıdaki formülü kullanmak gerekir:
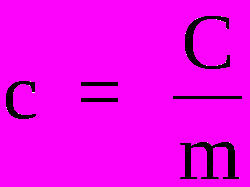
Nerede,
ç - özgül ısı (cal/g°C veya J/Kg.K)
Ç - termal kapasite (cal/°C veya J/K)
m - kütle (g veya kg)
Uluslararası Sistemde (SI), özgül ısı J/Kg cinsinden ölçülür. K (kilo başına joule ve kelvin başına). Ancak, en çok kullanılan ölçü cal/g°C (gram başına kalori ve santigrat derece başına kalori) cinsindendir.
Şuna da bakın: anlamı sıcaklık ve sıcaklık.