bu clapeyron denklemi gibi nicelikleri ilişkilendiren matematiksel bir ifadedir. basınç (P), hacim (V), sıcaklık (T) ve bir cismi oluşturan tanecik sayısı (n) mükemmel veya ideal gaz. Bu denklem, Fransız fizikçinin adını almıştır. Paulemileklapeyron ve ampirik yasaların bir genellemesi olarak anlaşılabilir. gazlarmükemmeliçindeGay-Lussac, Charles ve Boyle. İdeal gazların incelenmesi için temeldi ve evrimini mümkün kıldı. Termal makineler, onları son birkaç on yılda daha verimli hale getirdi.
Ayrıca bakınız: Kazayla Gerçekleşen Fizik Keşifleri
Clapeyron Denklemi: ideal gaz yasası
Clapeyron denklemi üç ampirik yasadan türetilmiştiryani deneylerden belirlenen yasalar. Bu tür yasalar gazların davranışını açıklar. gaz dönüşümleriizovolümetrik (Gay-Lussac yasası), izobarik (Charles yasası) ve izotermler (Boyle Kanunu). Bu yasalara göre:
dönüşümlerde izovolümetrikideal bir gazın basıncı ile termodinamik sıcaklığı arasındaki oran sabit kalır;
dönüşümlerde izobarik, ideal bir gazın hacmi ile termodinamik sıcaklığı arasındaki oran sabittir;
- dönüşümlerde izotermler, ideal bir gazın basınç ve hacminin çarpımı sabit kalır.
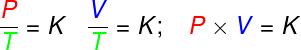
P – basınç (Pa – pascal)
V – gaz hacmi (m³)
T – termodinamik gaz sıcaklığı (K – kelvin)
Yukarıdaki üç yasadan, Clapeyron denklemi bunun değerinin ne olduğunu belirler. sabit (K) Yukarıda belirtilen dönüşümlerin her birinde elde edilen Clapeyron denklemine göre, bu sabit mol sayısının bir ile çarpımına eşittir. sabit Rideal gazların evrensel sabiti olarak bilinir ve şuna eşittir: Boltzmann sabiti çarpılır Avogadro'nun numarası.
formül
olarak bilinen formülü inceleyin. denklemiçindeKlapeyron:
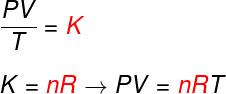
Hayır – mol sayısı (mol)
$ – ideal gazların evrensel sabiti (R = 0.082 atm.l/mol. K veya 8.314 J.mol/K)
Clapeyron denklemi incelendiğinde, basınç ideal gazların uyguladığı sıcaklıkla doğru orantılı ve ayrıca mol sayısı. Ayrıca, basınç hacimle ters orantılıdır gaz işgal etti.
Şimdi durma... Reklamdan sonra devamı var ;)
Ö ideal gaz modeli Clapeyron denkleminin mümkün kıldığı tarafından desteklenen makinelerin geliştirilmesi sıvılarbuharla çalışan makineler ve içten yanmalı motorlar gibi.
Clapeyron denkleminden birkaç önemli sonuç elde edilebilir. Örneğin bunlardan biri, herhangi bir ideal gazın 1 molünün bir hacim kapladığını tahmin ediyor. 22,4 litre baskısına maruz kaldığında 1 atm (1,01.105 Pa) ve sıcaklığında 273K (0°C).
Ayrıca bakınız: Termolojide En Önemli Kavramlar
Clapeyron Denklemi Üzerine Çözülmüş Alıştırmalar
Soru 1 —(UECE) Sıcaklığı, hacmi ve basıncı PV = nRT ile ilişkili olabilen bir gaz aşağıdaki özelliklere sahiptir:
a) çarpışma dışında moleküller arası etkileşimleri göz ardı etmek için moleküller arasındaki çok büyük ortalama mesafe; moleküller esnek çarpışmalara uğrarlar.
b) moleküller arasındaki çok küçük ortalama mesafe; Moleküller esnek olmayan çarpışmalara maruz kalır.
c) çarpışma dışında, moleküller arası etkileşimleri göz ardı etmek için moleküller arasındaki çok büyük ortalama mesafe; Moleküller esnek olmayan çarpışmalara maruz kalır.
d) moleküller arasında çok büyük ortalama mesafe ve güçlü moleküller arası etkileşimler; moleküller esnek çarpışmalara uğrarlar.
çözüm:
İdeal gaz modelinde çok sayıda boyutsuz parçacık rastgele yönlerde yüksek hızda hareket eder. Bu parçacıkların maruz kaldığı tek etkileşim, mükemmel esnek çarpışmalardır, bu nedenle doğru alternatif şudur: a harfi.
2. Soru —(UFRGS) İdeal gazlarla ilgili aşağıdaki ifadeleri inceleyiniz.
BEN. pV = nRT gazları için durum denkleminde bulunan R sabiti, tüm ideal gazlar için aynı değere sahiptir.
II. Aynı sıcaklık ve basınçta eşit hacimlerde farklı ideal gazlar aynı sayıda molekül içerir.
III. İdeal bir gazın moleküllerinin ortalama kinetik enerjisi, gazın mutlak sıcaklığı ile doğru orantılıdır.
Hangileri doğru?
a) Sadece ben
b) Yalnız II
c) Yalnız III
d) Sadece I ve II
e) I, II ve III
Şablon:
Alternatiflere bakalım:
BEN. doğru, bu nedenle ideal gazların evrensel sabiti olarak adlandırılır.
II. doğru. Clapeyron denklemine göre, iki ideal gaz aynı basınç, sıcaklık ve hacme sahipse, bu gazlardaki tanecik sayısı eşittir.
III. doğru. Enerji eş bölüşüm teoremine göre, ideal bir gazdaki parçacıkların kinetik enerjisi, sıcaklığıyla orantılıdır.
Bu nedenle, doğru alternatif, e harfi.
Soru 3 - (UFJF) Diğerlerinin yanı sıra Clapeyron, Boyle, Mariotte, Gay-Lussac, van der Walls gibi adamlar gazların özelliklerini içeren önemli çalışmalar geliştirmişlerdir. Gerçek gazların davranışı, düşük basınç koşullarında ideal gazlara ve ayrıca büyük hacimde bulunan gazlara ve yüksek sıcaklıklarda tutulan gazlara yakındır. Bir laboratuvar deneyinde, V hacmindeki bir kabın tamamen kapalı olduğunu ve 4.0 basınç altında 1 mol ideal gaz içerdiğini düşünün. atm, 127 ºC'ye eşit sabit bir sıcaklıkta genleşmeye maruz kalır ve bu gazın davranışı, şekilde gösterildiği gibi ideal bir gazın davranışıdır. grafik.
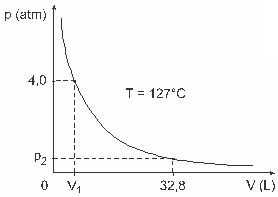
Bu durumda, gaz 32,8 L'ye eşit bir hacim işgal ettiğinde, gazın uyguladığı basınç şöyle olacaktır:
(Verilen: mükemmel gazların evrensel sabiti R = 0.082 atm'dir. L/mol. K.)
a) 0.32 atm
b) 0.40 atm
c) 1.0 atm
d) 2.0 atm
e) 2.6 atm
çözüm:
C harfi
Alıştırmayı çözmek için, verileri Clapeyron denklemine uygulamamız gerekiyor, ancak ondan önce santigrat derece cinsinden olan sıcaklığı kelvin'e dönüştürmemiz gerekiyor. Ödeme:

Rafael Hellerbock tarafından
Fizik öğretmeni

