metaller parlaklık, mukavemet, termal ve elektriksel iletkenlik ile karakterize edilen elemanlardır. Onlar hemen hemen tüm endüstriyel proseslerde uygulanabilir, aletlerin, mücevherlerin ve madeni paraların imalatında kullanılan metalik alaşımlarda ve redoks gibi kimyasal işlemlerde bulunur, yığınlar ve piller.
Periyodik Tabloda, bunlar şu şekilde sınıflandırılır:
yarı metaller
geçiş metalleri
alkali metaller
alkali toprak metalleri
Çelik endüstrisinde, bunlar ayrılır:
Demirli metaller
Demir olmayan metaller
ağır metaller
Siz de okuyun: Periyodik tablonun yeni unsurları nelerdir?
Metal özellikleri

Çoğunlukla mükemmel ısı ve elektrik enerjisi iletkenleridir.
Parlak bir görünüme sahiptirler.
yüksek yoğunluk.
Elektropozitif elementlerdir (katyon oluşturma eğilimindedirler - pozitif yükler).
hariç olmak üzere Merkür, erime noktası yüksek ve oda sıcaklığında katı olan elementlerdir.
Mekanik mukavemete (dayanıklılığa) sahiptirler.
Dövülebilirdirler (kırılmadan kalıplanabilirler).
Şimdi durma... Reklamdan sonra devamı var ;)
Periyodik Tablo Metalleri
alkali metaller
unsurlarıdır periyodik tablonun ilk sütunu, aile 1A. Alkali metaller olarak adlandırılırlar çünkü suyla karıştırıldıklarında hidroksitler, yani alkali (bazik) bir çözelti oluştururlar.
Sen elementler bu gruba ait olanlar:
Lityum (li)
Sodyum (At)
Potasyum (K)
Rubidyum (Rb)
Sezyum (Cs)
Francio (Fr)
Nötr (yüksüz/iyonize) durumdaki alkali metallerin elektronik konfigürasyonu yalnızca son kabukta bir elektron (değerlik katmanı). Ö atom ışını ve bu metallerin reaktivitesi yukarıdan aşağıya doğru artar (gözlemlenerek Periyodik tablo). Diğer metallere göre düşük bir erime noktasına sahiptirler, dövülebilir ve çok yoğun değildirler, mat bir görünüme sahiptirler. yüksek oksidasyon potansiyeli.
Ayrıca bakınız:Maddenin özellikleri nelerdir?
alkali toprak metalleri
Bunlar, ekranda görünen unsurlardır. periyodik tablonun ikinci sütunu, aile 2A. arandı Alkalin toprak bazik (alkali) karakterli çözeltiler oluşturma eğilimi ve toprak tarafından, çünkü 19. yüzyıldan önce bu maddelerin oluşturduğu oksitler bu şekilde belirlendi. Bu terim, ısıtıldığında mutasyona uğramayan çözünmeyen metalleri, grup 2 elementlerinin ortak özelliklerini belirtmek için kullanılmıştır. Daha sonra yeni araştırma ve deneyler ışığında "toprak" elementlerinin aslında metallerin oluşturduğu oksitler olduğu keşfedildi.
Düşük yoğunluklu, dövülebilir metallerdir. en dış kabuğunda iki elektron, normal sıcaklık ve basınç koşulları altında katı halde bulunur. Bu gruba ait:
Berilyum (Ol)
Magnezyum (Mg)
Kalsiyum (Buraya)
Stronsiyum (Bay)
Baryum (Ba)
Radyo (Kurbağa)
geçiş metalleri
telafi etmek Periyodik Tablonun B grubu, ve alkali toprak metalleri ile toprak arasında bulunur. ametaller. IUPAC tarafından tamamlanmamış bir energéticad' enerjik alt katmanına sahip elementler olarak tanımlandılar. Dönem "geçiş metalleri" anlamına gelir 2. gruptan 13'e geçiş Periyodik Tabloda ve 'd' orbitalinde artan elektron ilavesi.
Geçiş metali grubu, yüksek erime ve kaynama noktalarına sahip yoğun elementlerden oluşur ve grup 1 ve 2 metallerden daha az reaktif (Aile 1A ve 2A). Geçiş metalleri arasında ergime noktası en yüksek (3422 °C) element olan tungsten ve cıva (Hg) bulunur. normal sıcaklık ve basınç koşullarında sıvı halde olan bir metaldir, erime noktası (-38.83 °C)'dir.
Geçiş metallerinin çeşitli oksidasyon durumları vardır (NOX değişken) ve renkli maddeler oluşturur.

İç geçiş elemanları
İç geçiş elemanları onlar:
Lantanitler: 57 ila 71 protona sahip ve prometyum hariç doğal olan elementlerden oluşan seriler.
Aktinitler: atom numarası 89 ile 103 arasında değişen ve çoğu sentetik olan elementlerin oluşturduğu grup. Bu grubun hepsi radyoaktif kısa yarı ömrü ile.
Bu iki grubun elementleri yüksek bir erime noktasına sahiptir ve oda sıcaklığında hepsi katıdır.
yarı metaller
Sen yarı metaller toplamda yedi unsur vardır:
Bor (B)
Silikon (Si)
Germanyum (Ge)
Arsenik (As)
Antimon (Pzt)
Tellür (Te)
Polonyum (Po)
Bu sınıflandırma, sahip olan elemanlara verilir. metallerle ilgili fizikokimyasal özellikler ve ayrıca metalik olmayan elementlerle ilgili diğerleri. Yarı metaller parlaktır, kırılgan bileşiklerdir, anyonların yanı sıra katyonlar oluşturabilen (duruma bağlı olarak) ve ara iletkenlerdir.
Metal Çeşitleri
demir: bileşiminde demir içeren maddeler. Onlar metal alaşımları ortak bir element olarak demir içeren, ancak farklı konsantrasyonlarda formüle edilebilen karbon, örneğin, veya farklı tekniklerle dövülmüş, böylece farklı fiziksel özelliklere sahip ürünlere sahip olunmuştur.
demir dışı: gibi diğer metal türleri tarafından oluşturulan alaşımlar alüminyum, bakır, nikel, çinko, titanyum.
Ağır metaller: kurşun, nikel, çinko, cıva. Reaktif, toksik ve biyobirikimli metallerdir. Diğerlerinin yanı sıra pillerde, lambalarda, askeri eserler için mühimmatta kullanılırlar.
Metallerin kimyasal bağları
metaller elementler elektropozitifyani kimyasal bir bağda elektron kaybetme eğilimi gösterirler. Bir metal, ametalle etkileştiğinde, iyonik bağ yapmak farklılık nedeniyle elektronegatiflik. Metaller için diğer bir bağlanma olasılığı metal bağlarıdır.
at metal bağlantılar metaller arasında, elektronların kısmi salınımı ve atomların etrafında bir elektron bulutu veya denizi oluşumu ile meydana gelir, bu da metal parçaların özelliklerini garanti eder. iletkenlik elektrik ve dövülebilirlik.
Ayrıca bakınız: İletkenler ve yalıtkanlar - farklar nelerdir?
metal elde etmek
Çoğu metal doğal olarak bulunur diğer elementlerle ilişkili kayalar ve mineraller. Elektroliz ve kimyasal reaksiyonlar yoluyla bileşikleri ayırmak gibi metalleri arıtmak için çeşitli teknikler vardır.
Metaller söz konusu olduğunda, bir metalde belirli bir saflık derecesi elde etmek için endüstriyel ölçekte en çok kullanılan iki teknik şunlardır: farkı yoğunluk ve manyetik duyarlılık (metalin bir reaksiyona tepki verme eğilimi manyetik alan).

çözülmüş alıştırmalar
Soru 1 - (Enem) Pillerde bulunan kadmiyum, bu maddeler çevreye düzensiz olarak atıldığında veya yakıldığında toprağa ulaşabilir. Metalik formun aksine, Cd2+ iyonları, yerini alabilecekleri için vücut için son derece tehlikelidir. Ca2+ iyonları, kemiklerde dejeneratif bir hastalığa neden olarak onları çok gözenekli hale getirir ve kemiklerde şiddetli ağrılara neden olur. eklemler. Ayrıca böbreklerin çalışması için son derece önemli olan Zn2+ katyonu tarafından aktive edilen enzimleri de inhibe edebilirler. Şekil, bazı metallerin ve bunların ilgili katyonlarının yarıçapındaki değişimi göstermektedir.
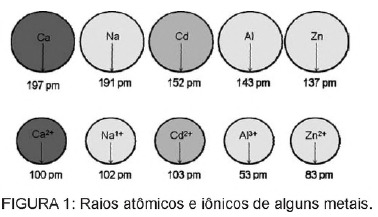
Metne dayanarak, kadmiyumun iyonik formundaki toksisitesi bu elementin bir sonucudur.
A) iyon oluşumunu destekleyen ve diğer bileşiklere bağlanmasını kolaylaştıran düşük iyonlaşma enerjisi sunar.
B) +1 ile +3 arasında değişen yüklere sahip metalik katyonların aracılık ettiği biyolojik süreçlerde hareket etme eğilimi vardır.
C) biyolojik süreçler üzerinde etki eden ve bu süreçlerde girişime neden olan metal iyonlarına nispeten yakın bir yarıçapa ve yüke sahiptir.
D) daha küçük iyonların normal olarak katıldığı biyolojik süreçlere müdahale etmesine izin veren büyük bir iyonik yarıçapa sahiptir.
E) normalde daha düşük yüklü iyonların katıldığı biyolojik süreçlere müdahale etmesine izin veren +2 yüke sahiptir.
çözüm
Alternatif C. Kadmiyum, vücudumuzda doğal olarak bulunan metalik iyonlara benzer bir elementtir. Metalik gruplara bu benzerliğe sahip olan kadmiyum, biyobirikimli olmasının yanı sıra moleküllerin sülfhidril gruplarına da bağlanabilir. Böylece dekalsifikasyon, doku ve kırmızı kan hücresi yıkımı gibi biyolojik süreçlerde değişikliklere neden olur. kan.
Soru 2 - Metallerle ilgili özellikler için yanlış seçeneği işaretleyin.
A) Çoğu metal iyi elektriksel ve termal iletkendir.
B) Bazı metaller oksidasyona ve/veya indirgenmeye karşı hassastır.
C) Demir, dayanıklı ve dövülebilir bir metaldir, yani kalıplanması kolaydır.
D) Alkali toprak metalleri, bu metallerin koyu renkli oksitlerine atıfta bulunarak “toprak” adını alır.
E) Metaller, oksidasyon etkisinden dolayı çeşitli renklerde ve donuk elementlerdir.
çözüm
Alternatif E. Metaller doğal olarak parlak ve metalik renktedirler, oksidasyona uğrayabilirler ve bu da metalle ilgili özelliklerde değişikliklere neden olur. parçanın yönü, ancak bu tüm metallerde meydana gelen bir fenomen değildir ve bazı durumlarda oksidasyon birkaç faktöre bağlıdır. harici.
tarafından Laysa Bernardes
Kimya hocası