at moleküller arası kuvvetler Kimyada Ulusal Lise Sınavında kesinlikle görünebilecek bir konudur (ve ya). Bu nedenle, bu makaledeki bu konunun ana içeriğini kontrol etmeye değer.
Tanım
moleküller arası kuvvetler bunlar, aralarındaki birliği koruyan bir maddenin molekülleri arasında kurulan elektrostatik çekim veya bağların - değişen yoğunluklarda (zayıf, orta veya güçlü) kuvvetleridir.
Moleküller arası kuvvet türleri
) indüklenmiş dipol
Ve moleküller arası kuvvet polar olmayan bir özelliğe sahip bir maddenin molekülleri arasında meydana gelen olay. Örneğin, O gibi maddelerin molekülleri arasında olur.2, H2, Hayır2, CO2, CH4.
Bu moleküller arasındaki birleşme, aralarında bir dipol oluştuğunda meydana gelir. Bu, bir molekülün elektronları diğerinin elektronlarını yer değiştirdiğinde ve böylece bir molekülden diğerine aktarılan bir negatif ve bir pozitif kutup oluşturduğunda olur.
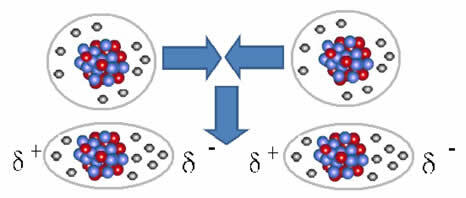
Polar olmayan moleküllerde dipol oluşumunun temsili
Bu moleküller arasında iki kutup oluşur ve birinin negatif kutbu diğerinin pozitif kutbu ile etkileşime girer. Bu kutuplar yaratıldığından, düşük yoğunluklu moleküller arası bir kuvvettir.
B) kalıcı dipol
Ve moleküller arası kuvvet Polar özelliği olan bir maddenin molekülleri arasında meydana gelen olay. Örnekler, HCN, H gibi maddelerin molekülleridir.2O, NH3, CO, CH3Cl.
Bu moleküller arasındaki birleşme, birinin negatif kutbu diğerinin pozitif kutbu ile etkileşime girdiğinde gerçekleşir.
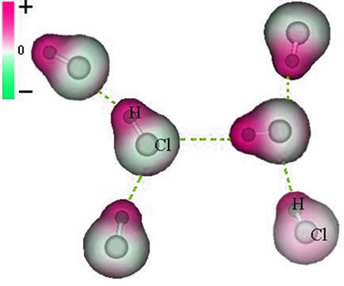
HCl molekülleri arasındaki kalıcı dipol kuvvetinin temsili
Kutuplar zaten mevcut olduğundan, kalıcı dipol moleküller arası kuvvet, indüklenen dipolden daha yoğundur.
ç) hidrojen bağları
bu moleküller arası kuvvet bir oksijen, nitrojen veya flor atomuna doğrudan bağlı bir hidrojen atomuna sahip polar moleküller arasında meydana gelir.
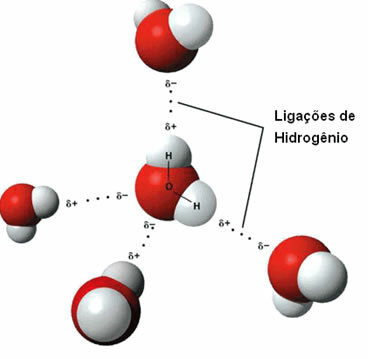
Su molekülleri arasındaki hidrojen bağlarının temsili
Bir moleküldeki hidrojen, diğer molekülün oksijen, azot veya flor ile etkileşime girdiğinde bir hidrojen bağı oluşur.
d) dipol iyonu
Bu moleküller arası kuvvet, bir çift bağ yapmayan elektrona sahip bir polar molekül ile çözeltideki bir iyon (katyon veya anyon) arasında meydana gelir.
Örneğin su molekülü oksijende iki çift bağlanmayan elektrona sahiptir. Sulu ortamda iyonlar varsa, içinde kutuplar olduğu için su molekülüne yakınlaşırlar.
Şimdi durma... Reklamdan sonra devamı var ;)
Önem
bilmenin önemi Enem için moleküller arası kuvvetler maddelerin fiziksel halleri, erime noktası, kaynama noktası ve çözünürlüğü hakkında getirdikleri anlayıştır.
) Maddenin erime ve kaynama noktası ile ilişkisi
Erime noktası, katıdan sıvı hale geçişin sıcaklığını, kaynama noktası ise sıvıdan gaz haline geçişin sıcaklığını gösterir.
Bu geçiş, maddenin molekülleri arasındaki etkileşimle doğrudan ilgilidir, çünkü bir fiziksel durumu diğerinden ayıran şey, molekülleri arasındaki kümelenme düzeyidir.
Bu nedenle, moleküller arası kuvvet ne kadar yoğun olursa, erime ve kaynama noktaları o kadar yüksek olur. Moleküller arası kuvvet ne kadar az yoğun olursa, erime ve kaynama noktaları o kadar düşük olur. Böylece, azalan erime ve kaynama noktası sırasını tanımlayabiliriz:
Hidrojen bağı > kalıcı dipol > indüklenmiş dipol
B) Çözünürlük ilişkisi
Genel olarak, benzerin benzerini çözdüğünü, yani polar maddenin polar maddeyi ve polar olmayan maddenin polar olmayan maddeyi çözdüğünü bilmeliyiz.
Bununla birlikte, çözünen moleküller ve çözücü moleküller arasında hala etkileşim olasılığı vardır. Bu, ancak bu yeni etkileşim, maddenin kendisinin molekülleri arasında zaten var olandan daha büyükse olur.
Enem'de moleküller arası kuvvet uygulaması örneği
1. Örnek: (Enem-2011) İnsan cildi iyi nemlendiğinde iyi bir elastikiyet kazanır, yumuşak ve pürüzsüz bir görünüm kazanır. Öte yandan kuruduğunda elastikiyetini kaybederek mat ve pürüzlü bir görünüm kazanır. Cilt kuruluğunu önlemek için mümkün olduğunda genellikle gliserin ve polietilen glikolden yapılmış nemlendirici nemlendiriciler kullanmak gerekir:

Nemlendiriciler tarafından cilt yüzeyinde su tutulması, ıslatıcı maddelerin hidroksil gruplarının çevrede bulunan nem ile etkileşiminin bir sonucudur:
a) iyonik bağlar
b) Londra kuvvetleri
c) kovalent bağlar
d) dipol-dipol kuvvetleri
e) hidrojen bağları
Bu sorunun cevabı hidrojen bağıdır, çünkü su molekülünde bir oksijen atomuna hidrojen bağı vardır. Aynı şey propilen glikol ve polietilen glikol molekülleri için de geçerlidir, bu tip moleküller arası kuvvetin ortaya çıkması için uygun bir koşuldur.
Benden Diogo Lopes Dias
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
GÜNLER, Diogo Lopes. "Düşmanda Moleküller Arası Kuvvetler"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/forca-intermoleculares-no-enem.htm. 27 Haziran 2021'de erişildi.