Ö amonyum nitrat NH moleküler formülüne sahip katı bir maddedir4ŞEHİR3 ve beyaz görünüm (saf olduğunda). oluşturulmuş tarafından iyonlar NH4+ (amonyum) ve HAYIR3- (nitrat), yanıcı değildir, ancak yüksek oranda oksitleyici ve reaktiftir. Bozunma reaksiyonu, ürün olarak büyük miktarda gaz üretir ve bu da, patlamalar meydana gelebileceğinden, bu ürünün uygun olmayan şekilde depolanmasını ciddi bir sorun haline getirir. Ve ayrıca tarımda yaygın olarak kullanılan gübre olarak.
Siz de okuyun: Doğal maddeler - doğadan kaynaklanan moleküller
Amonyum Nitrat Nedir?

Amonyum nitrat bu bir tuz NH iyonlarından oluşur4+ (amonyum) ve HAYIR3- (nitrat). Bu katı bir bileşiktir, ne zaman saf, beyaz renklidir. Tarımsal gübre olarak yaygın olarak kullanılmaktadır, ancak patlayıcı üretiminde de kullanılabilir. çok oksitleyici bir maddedir, sonra oksitleyici. Amonyum nitratın kaçak reaksiyonu, yüksek bir salınım üretir. gazlar, sebep olan patlayıcı etki.
Amonyum Nitratın Özellikleri
Molar kütle: 80.04336 g/mol.
İyonlardan oluşan tuz: amonyum (NH4+) ve nitrat (NO3-).
Görünüm: beyaz katı.
Güçlü oksitleyicidir.
Diğer maddelerle kolayca reaksiyona girer.
Yanıcı değildir.
Normal sıcaklık ve basınç koşulları için:
- yoğunluk: 1,73 g/cm³;
- kaynama noktası: 210 °C;
- erime noktası: 169.6 °C;
- suda çözünürlük derecesi: 216 g/100ml;
- pH: 5.5 (0.2M).
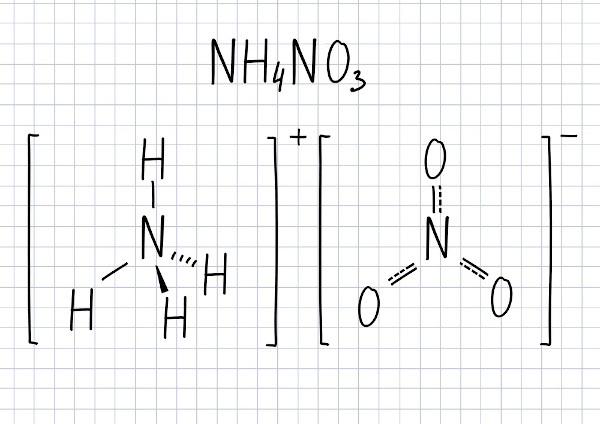
Amonyum Nitrat Formülü
Bu bileşiğin moleküler formülü NH'dir.4ŞEHİR3.
Amonyum nitratın ayrışması
olmak için yüksek reaktiviteye ve yüksek oksitleme potansiyeline sahip madde, amonyum nitrat, yüksek sıcaklığa maruz kaldığında, Ayrışma reaksiyonuve ana ürünler gazlar, azot, oksijen ve su buharı. Ayrıştırma iki adımda verilir:
→ 1. adım:
2NH4ŞEHİR3 (ler) → 2N20(g) + 4H2O(g)
→ 2. aşama:
2N2O → 2N2(g) + O2(g)
→ Küresel denklem:
2NH4ŞEHİR3 (ler) → 2N2(g) + O2(g) + 4H2O(g)
Dikkat edin, ilk denklemde,ürünlerden biri ayrıştırmada elde edilen azot oksit (N2Ö), Ayrıca şöyle bilinir gülme gazı. Özellikle diş hekimleri tarafından otomotiv motorlarının yakıt yakma gücünü artırmak ve anestezik olarak kullanılır. Ayrıca sorumlu gazlardan biridir. sera etkisi.
Ayrıca bakınız: Kimyasal reaksiyon türleri nelerdir?
Amonyum nitrat üretimi
Amonyum nitrat şu şekilde elde edilebilir: amonyum sülfat (NH4) arasındaki reaksiyon2SADECE4 ve kalsiyum nitrat Ca (NO3)2. Aşağıya bakınız:
(NH4)2SADECE4 + Ca (HAYIR3)2 → 2 NH4ŞEHİR3+ Kasa4
Gaz halindeki amonyaktan da üretilebilir.bir reaksiyon ürünü olarak sulu amonyum nitrata sahip olan bir nitrik asit çözeltisi içinde kabarcıklandırılan. Bak:
NH3(g) + HNO3(sulu) → NH4ŞEHİR3(İşte)
Amonyum Nitrat Kullanımları

- Gübre İmalatı
- Madenlerde, taş ocaklarında ve inşaatta patlayıcılar
- Herbisitler ve Böcek öldürücüler
- Endüstriyel uygulama için nitröz oksit elde edilmesi
- oksitler için emiciler
- Roket iticileri için oksitleyici
- İzotermal torba imalatı
- Arıcılıkta kovanların yönetimi için anestezik duman üretimi
Ayrıca erişim: Yangınla nasıl mücadele edilir?
Amonyum Nitrat Tehlikeleri
Amonyum nitratla ilişkili ana risklerden biri, yetersiz depolama. Çok oksitleyici bir madde olduğundan ve diğer birçok bileşikle reaksiyona girdiğinden, büyük miktarda gaz salınımı ile reaksiyon. Uygun olmayan depolama, yanıcı ürünlerle kontaminasyona, ısıya maruz kalmaya veya gaz tutulmasına, patlamalara ne sebep olabilir.
Bu, örneğin ABD'de Teksas'ta, Fransa'dan 2.086 ton amonyum nitrat taşıyan bir kargo gemisinde meydana geldi. kaza oldu 1947'de ve Texas City Afet olarak tanındı. Trajedi 581 kişinin ölümüne neden oldu amonyum kargosuna ulaşan gemide bulunmayan bir yangın sonucu meydana geldi ve patlamayı tetikledi.
Diğer bir örnek ise patlama sırası 4 Ağustos 2020'de limanda meydana gelen Beyrut şehri, Lübnan, 100'den fazla kişi öldü ve 5.000 kişi yaralandı. Patlamanın büyüklüğü, orada depolanan 2.750 ton amonyum nitratın kargosunun zincirleme reaksiyonunun ateşlenmesinden kaynaklandı.
Amonyum nitratın neden olabileceğini de belirtmekte fayda var. cilt ve göz tahrişi ve eğer solunursa, Solunum Problemleri. Kan dolaşımında madde vücut sıvılarıyla reaksiyona girdiği için toksik güce sahiptir ve bu reaksiyonun nitrat gibi ürünleri sağlığa zarar verebilir. mavi bebek hastalığı, infantil methemoglobinemi (düşük kan hemoglobini) olarak da bilinir. Bu hastalık, tarım bölgesindeki su kütlelerinin gübrelerde bulunan amonyum nitratla kirlenmesi nedeniyle kırsal alanlardaki ailelerde tekrarlar.
tarafından Laysa Bernardes
Kimya hocası
Kaynak: Brezilya Okulu - https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm


