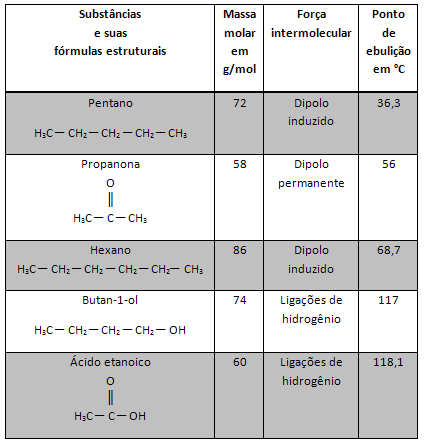
Atomlar, evrendeki tüm maddeyi oluşturan sonsuz küçük parçacıklardır. Zamanla, bilim adamlarının yaptığı yeni keşiflere göre atom yapısının nasıl olacağı fikri değişti. Bu konuda daha fazla bilgiyi metinde bulabilirsiniz.Atom Modelinin Evrimi.
Bir model, gerçekliğin bir temsilidir (gerçekliğin kendisi değil), bu nedenle atom modelleri, gerçekliğin temsilidir. atomun ana bileşenleri ve yapısı ve maddenin belirli fiziksel ve kimyasal davranışlarını açıklar. Bu yapılır çünkü bir insanın izole edilmiş bir atomu ultramikroskoplarla bile görmesi henüz mümkün değildir.
Atomun ne kadar küçük olduğu hakkında bir fikir edinmek için şunu bilin ki Sıradan bir mikroskop altında görülebilen en küçük parçacık, on milyardan fazla atom içerir! Atom o kadar küçük kiMilyonlarcasını yan yana koysak sonuca ulaşamayız. bir saçın kalınlığı.
Zihin Haritası: Atom
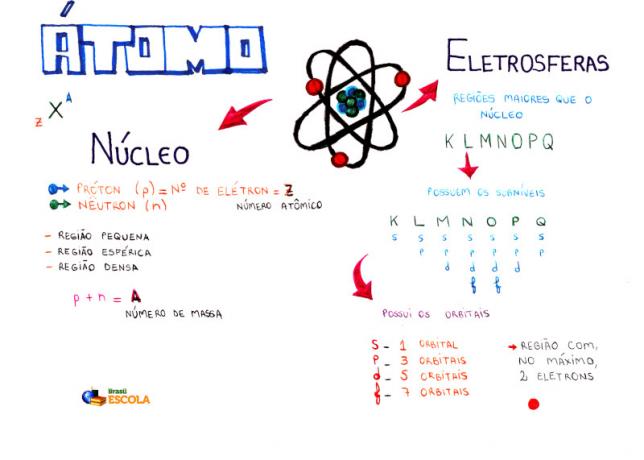
* Zihin haritasını PDF olarak indirmek için, Buraya Tıkla!
Atom modelleri arasında atomun yapısını ve özelliklerini anlamak için şu anda lisede en çok kullanılanı Rutherford-Bohr modelidir. Bu modele göre atomun yapısı iki ana bölümden oluşur:
çekirdek ve elektrosfer.
Bir atomun yapısının iki ana parçası - elektrosfer ve çekirdek
* çekirdek: Atomun merkezi kısmını oluşturan proton ve nötron olan daha büyük kütleli parçacıklardan oluşmanın yanı sıra kompakt, kütleli ve çok yoğundur.

Atom çekirdeğini oluşturan proton ve nötronların çizimi
- Protonlar: pozitif elektrik yüklü parçacıklardır (bağıl yük = +1; Coulomb cinsinden yük (C) = +1.602. 10-19) ve bağıl kütlesi 1'e eşittir.
Protonların çekirdeği oluşturduğu ve ona genel bir pozitif yük verdiği gerçeği, bilim adamları tarafından keşfedildi. Eugen Goldstein, 1886'da Crookes'un ampulünde bir değişiklik ve bazı deneyler yoluyla. Çok yüksek voltajlar altında emisyonların ortaya çıktığını gördü (anot ışınları - ampulün içindeki ve elektrik boşalmasıyla elektronlarını koparan gaz atomlarının kalıntıları). Ampulün dışına bir elektrik veya manyetik alan yerleştirerek, bu ışınlar negatif kutba doğru saptırıldı. Bu, proton denilen pozitif atom altı parçacıkların olduğu anlamına geliyordu.
Sonra, Ernest Rutherford (1871-1937) metinde açıklanan deneyi gerçekleştirdi Rutherford'un Atomu, bu da onu protonun yerini keşfetmeye yönlendirdi: çekirdekte.
- Nötronlar: protonların (1) kütlesine eşit olan parçacıklardır, ancak adından da anlaşılacağı gibi nötrdürler, yani elektrik yükleri yoktur.
1932 yılında nötronlar keşfedildi. James Chadwick (1891-1974), radyoaktif berilyum çekirdeğinin, kütlesi kabaca proton kütlesine eşit (aslında, biraz daha büyük) nötr parçacıklar yaydığını fark etti.
Şimdi durma... Reklamdan sonra devamı var ;)
Çekirdeğin çapı, atomun sahip olduğu proton ve nötron miktarına bağlıdır, ancak ortalama olarak 10 civarındadır.-14 ay ve 10-15 m.
Atom çekirdeği, çok küçük bir parçası olan atomun neredeyse tüm kütlesini yoğunlaştırır: hem proton hem de nötron, tüm atomun kendisinden yaklaşık 100.000 kat daha küçüktür! Karşılaştırma yoluyla, hidrojen elementinin atomunun çekirdeğini büyüttüğümüzü hayal edin (sadece bir proton) bir tenis topunun büyüklüğüne göre, en yakın elektron yaklaşık üç kilometre uzakta olacaktır. mesafe! Bir atom 14 katlı bir binanın yüksekliğine kadar büyütülse bile, çekirdeği yedinci kattaki sadece bir tuz tanesi büyüklüğünde olurdu. Bu gerçekten harika bir şey, sence de öyle değil mi?!
* Elektrosfer: Dır-dir elektronların çekirdek etrafında döndüğü bölge. Çekirdekten çok daha büyük hacimli bir bölge olmasına rağmen, her elektron 1 protondan (veya 1 nötrondan) 1836 kat daha küçük olduğu için pratik olarak boştur. Bu yüzden atomun kütlesi neredeyse tamamen çekirdektedir. Elektronlar, negatif elektrik yükü (-1) olan parçacıklardır.
Elektronlar 1897'de keşfedildi. Joseph John Thomson (1856-1940), yaratıcısı Thomson atom modeli. Thomson'ın deneyi metinde ayrıntılı olarak görülebilir. Thomson'ın elektrik deşarjları ile yaptığı deney, ama kısacası bahsi geçen Crookes ampulünü kullandı ve katot ışınlarının her zaman atomun negatif parçacıklara sahip olduğunu kanıtlayan pozitif kutup tarafından çekildi. elektronlar.
Elektronlar, çekirdeğin etrafında saniyenin milyonda birinde milyarlarca kez dönerek atomu şekillendirir ve katıymış gibi davranmasını sağlar.
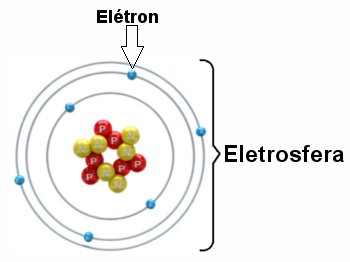
Üç elektronik katmana ve çekirdeğin etrafında dönen elektronlara sahip bir elektrosferin çizimi.
Kısaca, atomun yapısının bir parçası olan üç ana atom altı parçacığı ayırt etmek için bir tablo yapabiliriz:

Üç ana atom altı parçacığın kütlesi ve elektrik yükü - protonlar, nötronlar ve elektronlar
Tüm kimyasal elementlerin atomları bu üç atom altı parçacıktan oluşur. Bir kimyasal elementi diğerinden ayıran şey, bu parçacıkların görünme miktarı, özellikle atom numarası olarak adlandırılan çekirdekteki proton miktarıdır. Metin aracılığıyla bunun hakkında çalışmaya devam edin. Kimyasal element.
* Zihin Haritası Benden. Diogo Lopes
Jennifer Foğaça tarafından
Kimya mezunu
Kimya
Madde, su, hidrosiyanik gaz, karbondioksit, amonyak, hidrojen, helyum, maddelerin sınıflandırılması basit, bileşik maddeler, karışımlar, karışımın fazları, homojen karışım, karışım heterojen.