çalışmasında ideal gazlar Bir gazın, kinematik tarafından belirlenen yasalara göre hareket eden atomlardan ve moleküllerden oluştuğunu görüyoruz. Bir gazda, parçacıkları genellikle birbirinden çok uzaktadır ve aralarında boşluk vardır. Ayrıca gazların temel özelliğinin, pratik olarak yalnızca parçacıkları birbirleriyle çarpıştıklarında aralarında etkileşim olduğunu görüyoruz.
İdeal Gaz Yasası ile ilgili olarak bize basınç, hacim, sıcaklık ve mol sayısı arasındaki ilişkiyi gösterdiğini söyleyebiliriz. Bu ilişki, atomların ve moleküllerin hareketinin incelenmesine dayalı olarak makroskopik miktarlar arasındaki ilişkiyi belirlemeyi mümkün kılan basit bir gaz modelinden elde edilir. Gazların kinetik teorisi dört varsayıma dayanmaktadır:
1 – gaz düzensiz ve sürekli hareket halindeki moleküllerden oluşur. Her molekül diğerlerinden farklı bir hıza sahip olabilir.
2 – her gaz molekülü diğerleriyle yalnızca çarpışmalar (normal temas kuvvetleri) yoluyla etkileşir. Moleküllerin tek enerjisi kinetik enerjidir.
3 – Moleküller ve gazı içeren kabın duvarları arasındaki tüm çarpışmalar tamamen esnektir. Toplam kinetik enerji korunur, ancak her molekülün hızı değişebilir.
Şimdi durma... Reklamdan sonra devamı var ;)
4 – Moleküller sonsuz küçüktür. Bir gazın kapladığı hacmin çoğu boşluktur.
Bu varsayımlara dayanarak, Boltzmann ve Maxwell, ideal bir gazın toplam moleküllerinin ortalama kinetik enerjisinin, aşağıdaki ifadeye göre sıcaklıkla orantılı olduğunu gösterir:
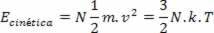
Burada k, Boltzmann sabitidir ve N, molekül sayısıdır. k değeri, gaz sabiti R ve Avogadro sayısı N'den hesaplanabilir.bu başına
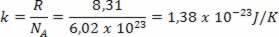
Elde edilen ifade, sıcaklığın ideal bir gazın moleküllerinin ortalama kinetik enerjisiyle orantılı olduğunu göstermektedir. Böylece, sıcaklığın bir gazdaki moleküllerin çalkalanma derecesinin ortalaması olduğunu görüyoruz. Mol sayısını kullanarak şunları elde ederiz:
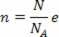
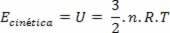
Domitiano Marques tarafından
Fizik Mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
SILVA, Domitiano Correa Marques da. "Gazların Kinetik Teorisi"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/fisica/teoria-cinetica-dos-gases.htm. 27 Haziran 2021'de erişildi.