DE saltbro föreslogs av den engelska kemisten Frederic Daniell, 1836, när denna forskare inrättade batteri uppkallad efter honom (Danills hög). den här bron är ett U-format rör som har två porösa ändar. (består av bomull eller agar-agar) och innehåller en vattenlösning bildad av vatten och ett salt. Det förbinder indirekt lösningarna på de två halva cellerna i cellen (anoden och katoden).
Observation: Anoden är den negativa polen i batteriet och det är där oxidation sker, och katoden är den positiva polen och där reduktion sker.
För att förstå saltbroens betydelse är det initialt nödvändigt att förstå pålens funktion. Se diagrammet nedan:
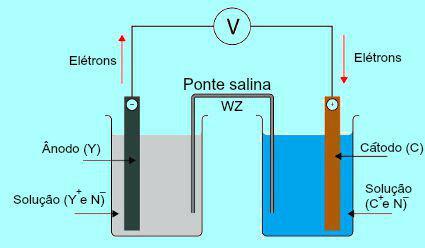
Allmänt schema för en Daniell stack
Initialt genomgår metallen (Y) på plattan som finns i anoden oxidation. När man genomgår oxidation förvandlas metallen till katjon som faller in i lösningen där plattan är. Av denna anledning börjar anodlösningen att presentera en högre koncentration av katjoner (Y+). I detta fall observeras en minskning av anodmetallplattan.
Y → och- + Y+
Därefter färdas elektronerna som förlorats under oxidationen av metoden i anodplattan genom den externa elektriska ledningen och går till metallplattan som finns i katoden. Således laddas plattan vid katoden med elektroner.
-
De nuvarande katjonerna (C+) i lösningen rör sig mot katodplattan eftersom den är laddad med elektroner. När katjonerna får elektroner som finns i plattan blir katjonerna neutrala (stabila och fasta) och fäster vid den. Av denna anledning uppvisar katodlösningen en högre koncentration av anjoner än katjoner. I detta fall observeras en ökning i storlek på katodmetallplattan.
Sluta inte nu... Det finns mer efter reklam;)
Ç+ + och- → C
Från förståelsen för hur Daniels högär det möjligt att observera att lösningen i anoden erhåller en större mängd Y-katjoner+ på grund av oxidationen av metallen på X-plattan. Lösningen som finns i katoden förlorar å andra sidan katjonerna (C+) eftersom de lider av minskning av plack.
Det är just i denna fråga som saltbryggans arbete lyfts fram. Huvudfunktionen för denna bro är att främja balansen mellan laddningar som finns i både anod- och katodlösningarna. I saltbryggan har vi alltid ett salt (vanligtvis kaliumklorid eller ammoniumnitrat.) Dissocierat i vatten. Se representationen av en ekvation i saltbryggan:
WZ + H2O → W+ + Z-
I saltbryggan finns två joner (W+ och Z-), som skiftas till katoden och anoden enligt:
De) Anoden tar emot anjonerna (Z-) närvarande i saltbryggan på grund av oxidationen av grundämnet (Y), vilket orsakar en ökning av mängden katjoner (Y+) i lösningen.
B) Katoden tar emot katjoner (W+saltbryggan eftersom katjonen (C. under batteridrift)+) som finns i lösningen reduceras på kortet. Således har katodlösningen en större mängd anjoner (N-) och får därför katjonen närvarande i saltbryggan.
Av mig Diogo Lopes Dias
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
DAGAR, Diogo Lopes. "Segelbro"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/ponte-salina.htm. Åtkomst den 28 juni 2021.


