Celler eller elektrokemiska celler och batterier är enheter där kemisk energi spontant omvandlas till elektrisk energi.Cellen består av bara två elektroder och en elektrolyt, medan batteriet är en serie batterier i serie eller parallellt.
På primära batterier är icke uppladdningsbara enheter, eftersom att när oxidationsreduktionsreaktionen som äger rum inuti dem upphör, måste de kasseras.
För varje utrustning anges en typ av batteri och bland de primära batterierna som för närvarande används är de viktigaste: Leclanché torra celler (vanliga batterier eller syra celler), alkaliska batterier och litium / mangandioxidbatterier.
Se vad som gör dem olika och vilken utrustning de är lämpliga för:
- Leclanché torra celler:
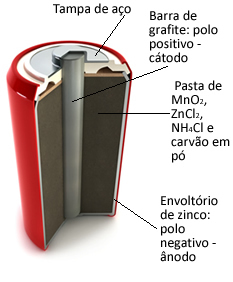
Dessa högar är i grunden bildade av ett zinkhölje, åtskilt av ett poröst papper och en central grafitstång omgiven av mangandioxid (MnO2kol, pulveriserat kol (C) och en våt pasta innehållande ammoniumklorid (NH4Cl), zinkklorid (ZnCl2) och vatten (H2O).
O zink fungerar som anod, förlorar elektroner; det är grafit fungerar som katod, ledande elektroner till mangandioxid:
Anodhalvreaktion: Zn (s) → Zn2+(här) + 2 och-
Katod halvreaktion: 2 MnO2 (aq) + 2 NH41+(här) + 2e- → 1 Mn2O3(s) + 2NH3 (g) + 1 timme2O(1)
Global reaktion: Zn (s) + 2 MnO2 (aq) + 2 NH41+(här) → Zn2+(här) + 1 Mn2O3 (s) + 2NH3 (g)
Denna typ av batteri är lämplig för utrustning som kräver lätt och kontinuerlig urladdning, såsom fjärrkontroll, väggklocka, bärbar radio och leksaker.
Du kan få mer information om ursprung, funktion, hållbarhet, ddp, faror och försiktighetsåtgärder som måste vidtas med dessa batterier i texten ”Leclanché Dry Stack”.
Sluta inte nu... Det finns mer efter reklam;)
- Alcaline-batterier:
Dess funktion är mycket lik den för Leclanché torra celler, men den enda skillnaden är den i stället för klorid ammonium (som är ett surt salt) tillsätts en stark bas, huvudsakligen natriumhydroxid (NaOH) eller kaliumhydroxid (KOH).
Anodhalvreaktion: Zn + 2OH → ZnO + H2O + 2e-
Katod halvreaktion: 2 MnO2 + H2O + 2e-→ Mn2O3 + 2 OH
Övergripande reaktion: Zn +2 MnO2→ ZnO + Mn 2O3

Alkaliska batterier är mer fördelaktiga än sura i den meningen att de har en större hållbarhet, t.ex. ger vanligtvis 50-100% mer ström än ett vanligt batteri av samma storlek, plus det finns mindre risk för läckage.
De indikeras huvudsakligen för enheter som kräver snabba och mer intensiva nedladdningar, till exempel radioapparater, bärbara CD / DVD- och MP3-spelare, ficklampor, digitalkameror etc.
Läs också texten Alcaline-batterier.
- Litium / mangandioxidbatterier:
Dessa batterier är lätta och genererar en stor spänning (cirka 3,4 V), varför de ofta används i liten utrustning som klockor och miniräknare. Till skillnad från tidigare fall är dess format valuta, vilket visas i följande bild:

Anoden är litium, katoden är mangandioxid och elektrolyten är en saltlösning:
Anod halv reaktion: läsa →läsa+ + och−
Katod halvreaktion: MnO2 + läs+ + och−→MnO2(li)
Övergripande reaktion: Li + MnO2 → MnO2(li)
Av Jennifer Fogaça
Examen i kemi
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FOGAÇA, Jennifer Rocha Vargas. "Vanligaste typer av celler och primära batterier"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/tipos-pilhas-baterias-primarias-mais-comuns.htm. Åtkomst den 27 juni 2021.

