Vad betyder det att säga att en gas har genomgått en gasformig omvandling?
För att svara på den ursprungliga frågan är det viktigt att komma ihåg att tillståndet för gas eller gasform bestäms av tillståndsvariablerna: tryck, volym och temperatur. Snart kommer en gasomvandling det är inget annat än någon situation där en viss mängd gas genomgår variation i en av dess tre tillståndsvariabler. Närhelst en variabel genomgår förändring kommer en annan att ändra sitt värde.
På 1600-talet genomförde flera forskare experiment för att upptäcka särdragen i gastransformationer. Bland dem kan vi nämna: Torriceli, Robert Boyle, Mariotte, Guericke, bland andra. I hans studier bestod förfarandet av att ändra en av tillståndsvariablerna och observera de andras beteende. Genom att göra detta observerade de att för att signifikant bestämma förhållandet mellan en variabel och en annan, det var nödvändigt att låta den tredje inte förändras, det vill säga att stanna kvar konstant. Således utfördes utredningarna på tre olika sätt, var och en med dess särdrag, de är:
isotermisk transformation, isobar transformation och isovolumetrisk transformation.Innan vi beskriver de tre ovan nämnda transformationerna, låt oss komma ihåg vad Allmän lag om perfekt gas: Enligt denna lag definierades en gasmassa initialt av tillståndsvariabler (s1, V1 och t1), när den genomgår en gasformig transformation har den tillståndsvariablerna (s2, V2 och t2) som karakteriserar gasens slutliga tillstånd. Dessa variabler följer följande förhållande:
Sluta inte nu... Det finns mer efter reklam;)

Från ovanstående ekvation kan vi se att tryck, volym och temperatur varierar under gastransformationen.
Isotermisk transformation ellerBoyle-Mariottes lag: är den transformation där temperaturen T av gasen förblir konstant och varierar dess tryck P och dess volym V. Följande lista är giltig:

Isobarisk transformation ellerGay-Lussac-lag: är den transformation där trycket P av gasen förblir konstant och varierar dess volym V och temperatur T. Följande lista är giltig:
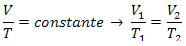
Isovolumetrisk transformation eller Charles Law: även känd som isometrisk transformation, är den transformation i vilken volymen V av gasen förblir konstant och varierar dess tryck P och temperatur T. Följande lista är giltig:

Av Nathan Augusto
Examen i fysik
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FERREIRA, Nathan Augusto. "Gastransformationer"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/fisica/as-transformacoes-gasosas.htm. Åtkomst den 27 juni 2021.