Kolatomen anses vara speciell för sin förmåga att bilda bindningar med andra atomer och ge upphov till långa kolkedjor. Allt beror på kolens tetravalens, det kan gå samman och bilda fyra bindningar, och de deltagande atomerna kan vara kol eller andra element. De senare kallas heteroatomer när de finns i kolkedjan.
De vanligaste heteroatomerna är: Kväve (N), Syre, Svavel (S) och Fosfor (P).
Exempel:
Syreatomen som finns i kedjan ovan är en heteroatom, som den är mellan kol.
Men se upp! Blanda inte förgrening med heteroatomkol, se:
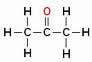
Syreatomen (i rött) är inte belägen mellan kol men över dem och bildar en gren, så den kan inte betraktas som en heteroatom.
Klassificering av atomer i en kolkedja:
I en kedja klassificeras varje kol enligt antalet andra kolatomer som är fästa vid det.
primärt kol: Fästs direkt på endast 1 annat kol.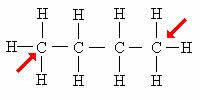
Pilen indikerar de primära kolerna. Observera att eftersom de ligger i ändarna av kolkedjan, binder dessa atomer till endast 1 kol.
sekundärt kol: Direkt kopplad till 2 andra kol.

De angivna kolerna är placerade mellan två kol.
tertiärt kol: Direkt kopplad till 3 andra kol.
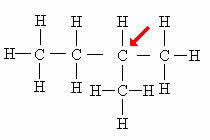
Observera att grenens närvaro (CH3) fäst vid den angivna atomen får den att få den tertiära kolklassificeringen.
Kvaternärt kol: Direkt kopplad till 4 andra kol.
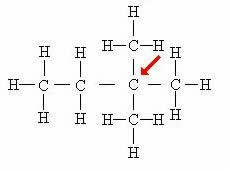
I detta fall bildar de fyra atomerna som är fästa vid det centrala kolet (indikerat av pilen) ett slags "fyrkant", vilket ytterligare bevisar närvaron av det kvaternära kolet.
Av Líria Alves
Examen i kemi
Brasilien skollag
Se mer!
Klassificering av kolkedjor: typer av bindningar
Egenskaper hos organiska föreningar
Organisk kemi - Kemi - Brasilien skola
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/capacidade-compostos-organicos-formar-cadeias.htm
