Eftersom det finns tusentals organiska föreningar kan fenomenet isomerism ta flera former. Därför kan isomerism i grunden klassificeras i två typer: platt eller konstitutionell isomerism och rymdisomerism eller stereoisomerism. Varje typ som nämns kan delas upp, som visas i följande diagram:
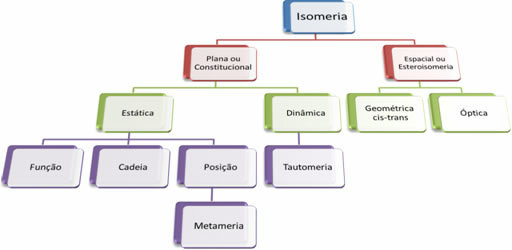
Se varje fall:
1. Platt eller konstitutionell isomerism: Isomerer av denna typ har samma molekylformel och differentieras med platta strukturformler. Det finns fem fall av planisomerism: funktion, kedja, position, metamerism och tautomerism.
1.1.Funktionell eller funktionell isomerism: Skillnaden mellan isomererna är i den funktionella gruppen.
Exempel: Molekylformel C3H6O
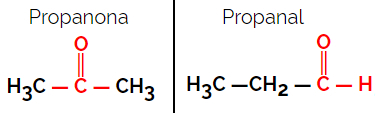
Observera att propanon kommer från ketongruppen och propanal är från aldehydgruppen.
1.2. Kedje- eller skelettisomerer: Skillnaden mellan isomererna är i typen av kedja. Exempelvis är en isomer öppen kedja och den andra sluten kedja, eller en är normal kedja och den andra grenade kedjan, eller en är en homogen kedja och den andra är en heterogen kedja.
Exempel: Molekylformel C4H10
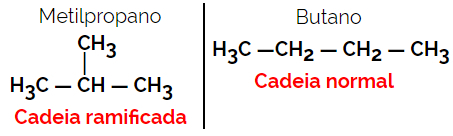
1.3.Positionell eller positionell isomerism: Skillnaden är i positionen för en omättnad, en funktionell grupp, en heteroatom eller en substituent.
Exempel: Molekylformel C4H6

1.4.Kompensationsisomerism eller metameri: Det är en speciell typ av positionisomerism, där skillnaden är placeringen av heteroatom.
Exempel: Molekylformel C4H10O
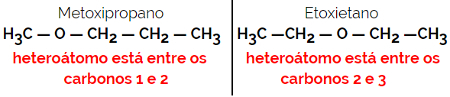
1.5.Dynamic Isomery eller Tautomery: Det är en speciell typ av funktionsisomerism, där isomererna samexisterar i dynamisk jämvikt i lösning. De två huvudtyperna av tautomeri är mellan en keton och enol (ketoenolbalans) och mellan en aldehyd och enol (aldoenolbalans).
Exempel: Molekylformel C3H6O
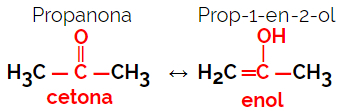
2. Rumsisomerism eller steroisomerism: I det här fallet kan skillnaden mellan isomererna bara visualiseras genom orienteringen av deras atomer i rymden. Det finns två typer av stereoisomerism: geometrisk isomerism och optisk isomerism.
2.1.Geometriska eller cis-trans-isomerer: Skillnaden är att isomeren heter cis den har samma kolligander i en dubbelbindning eller i cykliska föreningar på samma sida av planet. Isomerliganderna trans är på motsatta sidor.
Exempel: Molekylformel C2H2Cl2

Dessa föreningar kallas stereoisomerer.
2.2.Optisk isomer: Uppstår när isomerer kan avböja en stråle av polariserat ljus. Om den böjer den polariserade ljusstrålen till vänster är den en levorotär isomer, men om den böjs åt höger kallas den en högerhänt isomer.
Exempel:
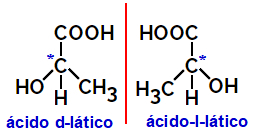
Asymmetriska molekyler som de som visas ovan, som är spegelbilder av varandra och som inte är överlagrade, kallas enantiomerer.
Av Jennifer Fogaça
Examen i kemi
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/tipos-isomeria.htm
