Vladimir Vasilyevich Markovnikov (1838-1904) var en kemiker i Moskva som 1869 började studera några reaktioner när man tillsatte vätehalogenider till alkener och alkyner.
I dessa reaktioner reagerar en alken med en vätehalogenid eller saltsyra, såsom väteklorid (HCl), vätebromid (HBr) och vätejodid (HI). Produkten bildad av alkenen är en alkylhalogenid, som vätebindningar till en av kolen i paret och halogenbindningar till den andra. Se exemplet nedan:
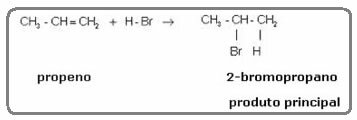
Något liknande förekommer också i hydratiseringsreaktionen hos alkener i ett surt medium; där den bildade produkten är en alkohol:
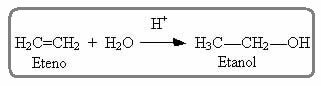
Den ovan nämnda etenmolekylen är symmetrisk; så det spelar ingen roll vilket kol vätet och halogenen tillsätts till. Men i asymmetriska molekyler, såsom propen, kan man förvänta sig bildandet av två möjliga produkter. Markovnikov såg dock att detta inte hände i praktiken. För att förstå, titta på reaktionen nedan:
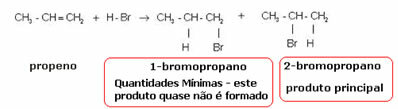
Produkten som bildas praktiskt taget ensam är 2-brompropan. Och Markovnikov såg att detta också gällde för andra ämnen. Så han formulerade följande regel:

Detsamma gäller för tillsats av vatten. Eftersom både vattenmolekylen och vätehalogeniderna är polära, så får dessa molekylers väte en elektropositiv karaktär.
Hδ+_ X δ- och Hδ+_ åh δ-
Att vara elektropositivt kommer väte att bindas till det mest elektronegativa kolet, vilket kommer att vara det som är bundet till den största mängden väte. Så vi har:
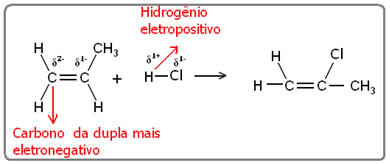
Av Jennifer Fogaça
Examen i kemi
Brasilien skollag
Källa: Brazil School - https://brasilescola.uol.com.br/quimica/regra-markovnikov.htm
